题目内容
14.在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述正确的是( )| A. | 白色沉淀是BaSO4和BaSO3 | B. | FeCl3全部被还原为FeCl2 | ||
| C. | 白色沉淀是BaSO3 | D. | 溶液的酸性减弱 |
分析 氯化铁具有强的氧化性,在酸性环境下能够氧化二氧化硫生成硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,硫酸根离子与钡离子发生反应生成硫酸钡沉淀,据此解答.
解答 解:氯化铁具有强的氧化性,在酸性环境下能够氧化二氧化硫生成硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,硫酸根离子与钡离子发生反应生成硫酸钡沉淀,
A、亚硫酸酸性弱于盐酸,与氯化钡不反应,所以不会产生亚硫酸钡沉淀,故A错误;
B、向过滤后的滤液中滴入KSCN溶液,无明显现象,说明溶液中三价铁离子全部被还原为二价铁离子,故B正确;
C、白色沉淀是BaSO4,故C错误;
D、由反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+可知,溶液的酸性增强,故D错误;
故选:B.
点评 本题考查了二氧化硫、三价铁离子的性质,明确相关物质的化学性质及发生的反应是解题关键,题目难度不大.

练习册系列答案
相关题目
2.下列反应的离子方程式书写正确的是( )
| A. | FeCl3溶液与Cu反应:Fe3++Cu═Fe2++Cu2+ | |
| B. | AgNO3溶液与NaCl反应:Ag++Cl-═AgCl↓ | |
| C. | Cu(OH)2与CH3COOH反应:OH-+H+═H2O | |
| D. | CaCO3与HNO3反应:CO32-+2H+═H2O+CO2↑ |
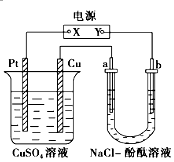 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法正确的是( )