题目内容
9.下列化学用语表示不正确的是( )| A. | S2-的结构示意图: | |
| B. | 乙烯的比例模型: | |
| C. | 乙醛的结构简式:CH3COH | |
| D. | 含中子数为10的氧元素的一种核素${\;}_8^{18}O$ |
分析 A.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构;
B.乙烯为平面结构,碳原子的相对体积大于氢原子;
C.醛基的表示方法错误,应该为-CHO;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数.
解答 解:A.S2-的最外层达到8电子稳定结构,其离子结构示意图为: ,故A正确;
,故A正确;
B.乙烯分子中含有1个碳碳双键,碳原子的相对体积较大,其比例模型为: ,故B正确;
,故B正确;
C.乙醛分子中含有1个醛基,其正确的结构简式为:CH3CHO,故C错误;
D.含中子数为10的氧元素的质量数=10+8=18,该核素可以表示为:${\;}_8^{18}O$,故D正确;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、元素符号、离子结构示意图、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题侧重考查学生的规范答题能力.

练习册系列答案
相关题目
18.元素X、Y、Z位于不同短周期,原子序数依次增大.X、Z同主族,二者的原子序数之和是Y原子序数的两倍.主族元素W的原子最外层电子数比电子层数多4.下列说汰不正确的是( )
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
20. 按如图装置进行实验,下列推断正确的是( )
按如图装置进行实验,下列推断正确的是( )
 按如图装置进行实验,下列推断正确的是( )
按如图装置进行实验,下列推断正确的是( )| 选项 | I中试剂 | II中试剂及现象 | 推断 |
| A | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
| B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
| C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油发生了化学变化 |
| D | 铁粉与水蒸气 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
| A. | A | B. | B | C. | C | D. | D |
17.向下列物质水溶液中通人过量的SO2后,最终既无沉淀也无气体产生的是( )
①H2S②NaHCO3③Na2SO3④Na2SiO3⑤Ba(NO3)2 ⑥Ca(OH)2 ⑦BaCl2.
①H2S②NaHCO3③Na2SO3④Na2SiO3⑤Ba(NO3)2 ⑥Ca(OH)2 ⑦BaCl2.
| A. | ①②④ | B. | ②③⑤ | C. | ③⑥⑦ | D. | ⑤⑥⑦ |
4.下列用途主要是体现铝的物理性质的是( )
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥炼钢的脱氧剂⑦做防锈油漆 ⑧做合金用作飞机制造业材料 ⑨工业做热交换器.
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥炼钢的脱氧剂⑦做防锈油漆 ⑧做合金用作飞机制造业材料 ⑨工业做热交换器.
| A. | ①②③④ | B. | ③④⑥⑦⑧⑨ | C. | ①③⑤⑦⑧⑨ | D. | ①③②④⑥⑧ |
1.下列电离方程式不正确的是( )
| A. | Ca(OH)2═Ca2++2OH- | B. | KNO3═K++NO3- | ||
| C. | H2SO4═2H++SO42- | D. | Na2SO3═Na2++SO42- |
18.实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:
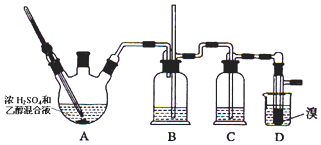
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.有关数据列表如下:
回答下列问题:
(1)写出三颈烧瓶A中发生反应的化学方程式CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O;
(2)为了减少A装置中副反应的发生,操作时应注意迅速地把反应温度提高到170℃左右;
(3)B装置的作用为平衡气压,以获得较平稳的气流,防止倒吸,判断装置是否堵塞;
(4)在装置C中应加入NaOH溶液,除去反应中可能生成的某些杂质气体,防止对后续实验造成干扰;
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.

可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132[ | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)写出三颈烧瓶A中发生反应的化学方程式CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O;
(2)为了减少A装置中副反应的发生,操作时应注意迅速地把反应温度提高到170℃左右;
(3)B装置的作用为平衡气压,以获得较平稳的气流,防止倒吸,判断装置是否堵塞;
(4)在装置C中应加入NaOH溶液,除去反应中可能生成的某些杂质气体,防止对后续实验造成干扰;
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
19.下列各组三种元素中,属于同一周期的是( )
| A. | C、H、O | B. | F、Cl、Br | C. | Li、Mg、B | D. | Si、S、P |
 甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径.由CO2制备甲醇过程可能涉及反应如下:
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径.由CO2制备甲醇过程可能涉及反应如下: