题目内容
1.下列化合物不属于天然高分子化合物的是( )| A. | 淀粉 | B. | 油脂 | C. | 纤维素 | D. | 蛋白质 |
分析 高分子化合物(又称高聚物)一般相对分子质量高于10000,结构中有重复的结构单元;有机高分子化合物可以分为天然有机高分子化合物(如淀粉、纤维素、蛋白质天然橡胶等)和合成有机高分子化合物(如聚乙烯、聚氯乙烯等).
解答 解:A.淀粉是多糖,相对分子质量在一万以上,为天然高分子化合物,故A不选;
B.油脂,相对分子质量较小,不是高分子化合物,故B选;
C.纤维素是多糖,相对分子质量在一万以上,为天然高分子化合物,故C不选;
D.蛋白质,相对分子质量在一万以上,为天然高分子化合物,故D不选.
故选B.
点评 本题考查高分子化合物判别,明确物质的成分及相对分子质量即可解答,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.已知乙烯和丙烯的混合物的质量为m g,NA代表阿伏加德罗常数,则该混合物( )
| A. | 所含共用电子对数目为($\frac{m}{7}$+1)NA | B. | 所含碳氢键数目为$\frac{m{N}_{A}}{7}$ | ||
| C. | 燃烧时消耗的O2一定是33.6m/14 L | D. | 所含原子总数为$\frac{m{N}_{A}}{14}$ |
6.如表是元素周期表的一部分,按要求填空( 填元素符号或化学式):
(1)写出①元素的元素名称碳.
(2)写出⑩元素的元素符号S.
(3)⑨在元素周期表中的位置:第三周期,第ⅤA族.
(4)在这些元素中,Na是最活泼的金属元素;F是最活泼的非金属元素;Ar是最不活泼的元素.(用元素符号填写)
(5)能形成气态氢化物,且气态氢化物最稳定的是HF.(用化学式填写)
(6)这些元素的最高价氧化物对应水化物中最强的酸是HClO4;最强的碱是NaOH;具有两性的氢氧化物是Al(OH)3.(用化学式填写)
(7)从⑤到⑪的元素中,Cl原子半径最小.(用元素符号填写)
(8)比较⑤与⑥的化学性质,Na更活泼(用元素符号填写),试用实验证明此现象(简述实验操作、现象和结论)分别将钠和镁投入冷水中,钠剧烈反应,镁缓慢反应,说明钠金属性比镁强.
(9)用电子式表示元素④与⑥形成的化合物: ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出⑩元素的元素符号S.
(3)⑨在元素周期表中的位置:第三周期,第ⅤA族.
(4)在这些元素中,Na是最活泼的金属元素;F是最活泼的非金属元素;Ar是最不活泼的元素.(用元素符号填写)
(5)能形成气态氢化物,且气态氢化物最稳定的是HF.(用化学式填写)
(6)这些元素的最高价氧化物对应水化物中最强的酸是HClO4;最强的碱是NaOH;具有两性的氢氧化物是Al(OH)3.(用化学式填写)
(7)从⑤到⑪的元素中,Cl原子半径最小.(用元素符号填写)
(8)比较⑤与⑥的化学性质,Na更活泼(用元素符号填写),试用实验证明此现象(简述实验操作、现象和结论)分别将钠和镁投入冷水中,钠剧烈反应,镁缓慢反应,说明钠金属性比镁强.
(9)用电子式表示元素④与⑥形成的化合物:
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
13.下列推断正确的是( )
| A. | CO2和CH4都是引起“温室效应”的气体 | |
| B. | Na2O、Na2O2的组成元素相同,但阳离子和阴离子的数目比不同 | |
| C. | SO2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 分别向新制氯水和久置氯水中滴加少量紫色石蕊试液,充分振荡后溶液都呈红色 |
10.证明海带中含有碘元素的实验方案如下,请你按要求补充完整:
| 步骤 | 实验过程 | 实验用品 |
| I | 将干海带灼烧灰化 | 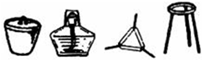 |
| II | 将海带灰溶解、过滤 | 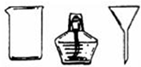 和①玻璃棒 和①玻璃棒 |
| III | 氧化滤液中的I-,反应的离子方程式为②2I-+H2O2+2H+=I2+2H2O | 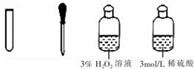 |
| IV | 取少量III中反应后溶液于试管中,加入少量CCl4并振荡后静置,观察到③下层溶液变为紫红色,说明海带中含有碘元素 |  |
11.下列是各烃的分子式,其中同分异构体只有三种的是( )
| A. | C3H8 | B. | C3H6 | C. | C4H10 | D. | C5H12 |
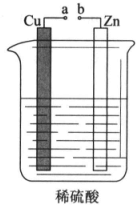 课外小组的同学对如图所示的实验装置进行了研究.
课外小组的同学对如图所示的实验装置进行了研究.