题目内容
下列热化学方程式中ΔH代表燃烧热(25℃,101 kPa)的是
A.CH4(g)+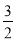 O2(g)
O2(g)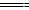 2H2O(l)+CO(g)ΔH1
2H2O(l)+CO(g)ΔH1
B.2CO(g)+O2(g)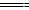 2CO2(g)ΔH2
2CO2(g)ΔH2
C.S(s)+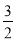 O2(g)
O2(g)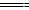 SO3(s)ΔH3
SO3(s)ΔH3
D.C6H12O6(s)+6O2(g)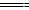 6CO2(g)+6H2O(l)ΔH4
6CO2(g)+6H2O(l)ΔH4
练习册系列答案
相关题目
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA | |
| B. | 常温下,46 g分子式为C2H6O的物质中一定含有极性键为7NA,非极性键为NA | |
| C. | 125 mL 16 mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于NA | |
| D. | 标准状况下,体积为22.4 L NO2、N2O4的混合气体,升温至常温,则混合气体分子数为NA |
13.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于电解质的是BCD.
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为0.1 mol/L.
(3)配制上述“鲜花保鲜剂”用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500mL容量瓶,胶头滴管(填写所缺仪器的名称).
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是⑤①④⑥③⑦②(填序号).
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度偏大(填偏大、偏小、不变).
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 3.48 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 1.58 | 158 |
| 硝酸银 | 0.02 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为0.1 mol/L.
(3)配制上述“鲜花保鲜剂”用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500mL容量瓶,胶头滴管(填写所缺仪器的名称).
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是⑤①④⑥③⑦②(填序号).
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度偏大(填偏大、偏小、不变).
11.某学生用0.1032mol•L-1的盐酸标准溶液滴定未知浓度的KOH溶液,其操作分解为如下几步:
A.取已用蒸馏水洗净的酸式滴定管,用盐酸标准溶液润洗滴定管2~3次;
B.移取20mL待测KOH注入洁净的锥形瓶中,并加入2~3滴甲基橙;
C.取标准盐酸溶液注入酸式滴定管至“0”刻度以上1~2cm;
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
E.调节液面至“0”或“0”以下某一刻度,记录读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记录滴定管液面的刻度.
完成下列问题:
(1)上述操作步骤的正确顺序是ACDEBF(填写字母序号).
(2)判断溶液到达滴定终点的方法是当溶液由黄色变为橙色,且在半分钟内不褪色.
(3)上述A步骤操作的目的是滴定管用蒸馏水洗涤后,内壁有一层水膜,如果直接装液会使浓度降低.
(4)若上述B步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果产生的影响是偏高;若称取一定量的KOH固体(含少量NaOH)配制待测溶液并用上述盐酸标准溶液进行滴定,则对滴定结果产生的影响是偏高,理由是因为同质量的NaOH比KOH中和能力强,消耗的盐酸多.
(5)用0.1032mol•L-1的盐酸滴定未知浓度的KOH溶液,重复三次的实验数据如下表所示:
则待测KOH的物质的量浓度是0.1124mol•L-1.
A.取已用蒸馏水洗净的酸式滴定管,用盐酸标准溶液润洗滴定管2~3次;
B.移取20mL待测KOH注入洁净的锥形瓶中,并加入2~3滴甲基橙;
C.取标准盐酸溶液注入酸式滴定管至“0”刻度以上1~2cm;
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
E.调节液面至“0”或“0”以下某一刻度,记录读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记录滴定管液面的刻度.
完成下列问题:
(1)上述操作步骤的正确顺序是ACDEBF(填写字母序号).
(2)判断溶液到达滴定终点的方法是当溶液由黄色变为橙色,且在半分钟内不褪色.
(3)上述A步骤操作的目的是滴定管用蒸馏水洗涤后,内壁有一层水膜,如果直接装液会使浓度降低.
(4)若上述B步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果产生的影响是偏高;若称取一定量的KOH固体(含少量NaOH)配制待测溶液并用上述盐酸标准溶液进行滴定,则对滴定结果产生的影响是偏高,理由是因为同质量的NaOH比KOH中和能力强,消耗的盐酸多.
(5)用0.1032mol•L-1的盐酸滴定未知浓度的KOH溶液,重复三次的实验数据如下表所示:
| 序号 | 消耗盐酸的体积/mL | 待测KOH溶液的体积/mL |
| 1 | 27.23 | 25.00 |
| 2 | 28.24 | 25.00 |
| 3 | 27.25 | 25.00 |


 2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是
2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是 23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。
23个水分子中,含分子数最多的是(填序号,下同)________,含原子数最多的是________,质量最大的是________,体积最小的是______。