题目内容
下列物质中含有离子键的是( )
| A、Br2 |
| B、CO2 |
| C、NH4Cl |
| D、HNO3 |
考点:离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:一般来说,活泼金属与非金属形成离子键,但铵盐中也存在铵根离子与酸根离子形成的离子键,以此来解答.
解答:
解:A.只含Br-Br共价键,故A不选;
B.只含C=O共价键,故B不选;
C.含铵根离子与氯离子之间的离子键和N-H共价键,故C选;
D.只含N、O与H、O之间的共价键,故D不选;
故选C.
B.只含C=O共价键,故B不选;
C.含铵根离子与氯离子之间的离子键和N-H共价键,故C选;
D.只含N、O与H、O之间的共价键,故D不选;
故选C.
点评:本题考查化学键,为高频考点,把握化学键判断的一般规律及特殊物质中的化学键为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列分子中的14个碳原子不可能处在同一平面上的是( )


| A、①③ | B、①②③ |
| C、①③④ | D、①②③④ |
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A、常温常压下,22.4 L Cl2与足量的铁粉反应,转移的电子数目为2NA |
| B、常温常压下,4 g CH4含有NA个C-H键 |
| C、常温常压下,92 g的NO2和N2O4混合气体中含有的原子数目为6NA |
| D、分子总数为NA的SO2和CO2混合气体中含有的氧原子数目为2NA |
从硫化物中提取单质锑(Sb)是先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe→Sb4O6+6FeS ②Sb4O6+6C→4Sb+6CO↑
Sb2S3和Sb4O6中Sb都为+3价.下列叙述正确的是( )
①2Sb2S3+3O2+6Fe→Sb4O6+6FeS ②Sb4O6+6C→4Sb+6CO↑
Sb2S3和Sb4O6中Sb都为+3价.下列叙述正确的是( )
| A、反应①中的氧化剂是Sb2S3 |
| B、反应②中还原剂是Sb4O6 |
| C、反应①中每生成3 mol FeS,转移6 mol电子 |
| D、反应②说明高温下C的还原性比Sb强 |
下列实验操作或原理不正确的是( )
| A、纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| B、抽滤时,滤纸要小于布氏漏斗 |
| C、重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
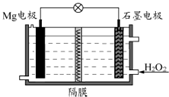 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )| A、Mg 电极是该电池的负极 |
| B、H2O2 在石墨电极上发生还原反应 |
| C、石墨电极附近溶液的pH 增大 |
| D、溶液中Cl-向正极移动 |
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).不能判断该分解反应已经达到化学平衡的是( )
| A、密闭容器中二氧化碳的体积分数不变 |
| B、密闭容器中气体的总物质的量不变 |
| C、密闭容器中混合气体的密度不变 |
| D、v(NH3)正=2 v(CO2)逆 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol由CO2和O2组成的混合物气体中含氧原子数为2NA |
| B、0.012千克石墨晶体中含共用电子对数目为2NA |
| C、标准状况下,NA个SO3分子所占的体积约为22.4L |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极溶解的铜的质量为64g |