题目内容
18.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA | |
| B. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| C. | 7.80 g Na2O2与5.85 g NaCl所含阴离子数相等 | |
| D. | 常温常压下,18g H2O含有的氢原子数为3NA |
分析 A、氯气和水的反应为可逆反应;
B、铜只能和浓硫酸反应,和稀硫酸不反应;
C、求出过氧化钠和氯化钠的物质的量,然后根据过氧化钠由2个阳离子和1个阴离子构成、而氯化钠由一个阳离子和一个阴离子构成来分析;
D、求出水的物质的量,然后根据水中含2个氢原子来分析.
解答 解:A、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于0.1NA个,故A错误;
B、铜只能和浓硫酸反应,和稀硫酸不反应,故浓硫酸不能反应完全,则生成的二氧化硫分子个数小于0.46NA个,故B错误;
C、7.8g过氧化钠和5.85g氯化钠的物质的量均为0.1mol,而过氧化钠由2个阳离子和1个阴离子构成、而氯化钠由一个阳离子和一个阴离子构成,故0.1mol过氧化钠和0.1mol氯化钠中均含0.1NA个阴离子,故C正确;
D、18g水的物质的量为1mol,而水中含2个氢原子,故1mol水中含2NA个氢原子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
9.2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关${\;}_{53}^{131}$I(碘-131)的相关报道成为热门话题.${\;}_{53}^{131}$I是常规核裂变产物之一,可以通过测定${\;}_{53}^{131}$I的含量变化来监测核电站放射性物质的泄漏情况,下列有关${\;}_{53}^{131}$I的叙述中错误的是( )
| A. | ${\;}_{53}^{131}$I的化学性质与${\;}_{53}^{127}$I相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的原子核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I的原子核内中子数多于质子数 |
13.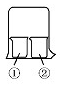 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( ) | ①中的物质 | ②中的物质 | 预测①的现象 | |
| A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
| A. | 淀粉KI溶液浓硝酸无明显变化 | B. | 酚酞溶液浓盐酸无明显变化 | ||
| C. | AlCl3溶液浓氨水有白色沉淀 | D. | 湿润红纸条饱和氯水红纸条褪色 |
10.下列物质中,不能用酸性KMnO4溶液鉴别,但可用溴水鉴别的是( )
| A. | 己烷 苯 | B. | 己烯 苯 | C. | 己烯 甲苯 | D. | 己烷 己烯 |
7.下列指定反应的离子方程式正确的是( )
| A. | 用醋酸溶解大理石:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| C. | 向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| D. | 亚硫酸钠溶液中滴加酸性高锰酸钾溶液:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
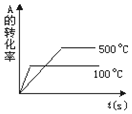
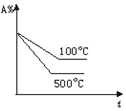
 (1)已知如图所示的可逆反应:
(1)已知如图所示的可逆反应: