题目内容
2.下表中对应关系正确的是( )| A | 由蛋白质得到氨基酸 由淀粉得到葡萄糖 | 均发生了水解反应 |
| B | CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| C | 2Na2O2+2H2O═4NaOH+O2↑ Cl2+H2O═HCl+HClO | 均为水作还原剂的氧化还原反应 |
| D | Cl2+2Br-═2Cl-+Br2 Zn+Cu2+═Zn2++Cu | 均为单质被还原的置换反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.蛋白质水解生成氨基酸,淀粉水解生成葡萄糖;
B.CH2=CH2+HCl→CH3CH2Cl中双键转化为单键,为加成反应;
C.2Na2O2+2H2O═4NaOH+O2↑、Cl2+H2O═HCl+HClO中,水不是氧化剂,也不是还原剂;
D.Cl2+2Br-═2Cl-+Br2中单质被还原,Zn+Cu2+═Zn2++Cu中单质被氧化.
解答 解:A.蛋白质水解生成氨基酸,淀粉水解生成葡萄糖,则均发生水解反应,故A正确;
B.CH2=CH2+HCl→CH3CH2Cl中双键转化为单键,为加成反应,而为取代反应CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl,故B错误;
C.2Na2O2+2H2O═4NaOH+O2↑中Na2O2为氧化剂和还原剂、Cl2+H2O═HCl+HClO中Cl2为氧化剂和还原剂,水均不是氧化剂,也不是还原剂,故C错误;
D.Cl2+2Br-═2Cl-+Br2中氯气得到电子被还原,Zn+Cu2+═Zn2++Cu中Zn失去电子被氧化,故D错误;
故选A.
点评 本题考查有机物的结构与性质及氧化还原反应,为高频考点,把握官能团与性质的关系、氧化还原反应中基本概念为解答的关键,侧重分析与应用能力的考查,注意反应类型的判断,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
19.下列说法中正确的是( )
| A. | 物质的量就是物质的质量 | |
| B. | 阿伏加德罗常数就是6.02×1023 | |
| C. | 1mol某物质溶于水一定得阿伏加德罗常数个溶质分子 | |
| D. | 98gH2SO4的物质的量与98gH3PO4的物质的量相等 |
10.LED产品的使用为城市增添色彩.下图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
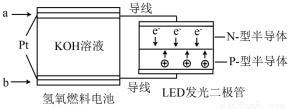

| A. | P一型半导体连接的是电池负极 | |
| B. | b 处通入O2为电池正极,发生了还原反应 | |
| C. | 通入O2的电极发生反应:O2+4e-+4H+=2H2O | |
| D. | 该装置只涉及两种形式的能量转换 |
17.某烃分子中有一个由碳碳单键构成的六元环,有一个碳碳双键,还有一个碳碳叁键,则能满足上述条件的烃的分子式可能是( )
| A. | C8H8 | B. | C10H16 | C. | C14H22 | D. | C12H22 |
7.2012年6月16日18点37分21秒,神舟九号载人飞船发射成功,与天宫一号目标飞行器进行首次载人空间交会手控对接,使中国的探月工程又迈出重要的一步.据预测,月球的土壤中吸附着数百万吨的氦23He,可作为未来核聚变的重要原料之一.对23He原子的叙述不正确的是( )
| A. | 质量数是3 | B. | 质子数是3 | C. | 中子数是1 | D. | 电子数是2 |
14.下列说法中错误的是( )
| A. | 食盐可作为调味剂、食品防腐剂,还可用于调节体液电解质平衡 | |
| B. | 碘是人体必需的影响智力发育的微量元素,但也不能摄入过多 | |
| C. | 油脂是高能量营养物质,肥胖者不能食用 | |
| D. | 面粉中添加适量的小苏打后做成馒头,既无酸味又疏松可口 |
11.一定条件下,可逆反应N2+3H2═2NH3(放热反应) 达到平衡后,只改变一个条件,下列叙述错误的是( )
| A. | 加催化剂,v正、v逆 都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆 都增大,且v正 增大的倍数大于V逆增大的倍数 | |
| C. | 增大氮气的浓度,H2的平衡转化率增大 | |
| D. | 降温,v正、v逆 都减小,且v正 减小的倍数大于v逆减小的倍数 |
12.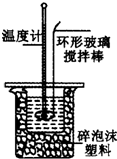 某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
I.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从如表中选择称量NaOH固体所需要的仪器是(填字母):
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
(3)取50mL.NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①上表中的温度差平均值为4.0℃;
②近似认为0.50mol/L NaOH溶液和O.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则中和热△H-53.5kJ/mol (取小数点后一位).
③上述实验数值结果与57.3kJ•mol叫有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
 某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.I.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从如表中选择称量NaOH固体所需要的仪器是(填字母):
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(3)取50mL.NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.6 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol/L NaOH溶液和O.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃),则中和热△H-53.5kJ/mol (取小数点后一位).
③上述实验数值结果与57.3kJ•mol叫有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.