题目内容
下列叙述正确的是( )
| A、熔融NaCl可以导电,则其溶液是电解质 |
| B、O3既不是电解质又不是非电解质 |
| C、CO2溶于水能导电,但CO2是非电解质 |
| D、BaSO4几乎不导电,是非电解质 |
考点:电解质与非电解质
专题:离子反应专题
分析:A.氯化钠的溶液为混合物,不属于电解质;
B.臭氧为单质,单质和混合物既不是电解质,也不是非电解质;
C.二氧化碳的水溶液导电的离子不是二氧化碳自身电离的,二氧化碳所以非电解质;
D.硫酸钡在熔融状态下能够导电,硫酸钡为电解质,且为强电解质.
B.臭氧为单质,单质和混合物既不是电解质,也不是非电解质;
C.二氧化碳的水溶液导电的离子不是二氧化碳自身电离的,二氧化碳所以非电解质;
D.硫酸钡在熔融状态下能够导电,硫酸钡为电解质,且为强电解质.
解答:
解:A.电解质不是为化合物,氯化钠的溶液为混合物,不属于电解质,故A错误;
B.臭氧为单质,单质既不是电解质,也不属于非电解质,故B正确;
C.二氧化碳溶于水能够导电,但是导电的离子不是二氧化碳电离的,所以二氧化碳为非电解质,故C正确;
D.硫酸钡的水溶液几乎不导电,但是硫酸钡在熔融状态下能够导电,硫酸钡所以电解质,且属于强电解质,故D错误;
故选BC.
B.臭氧为单质,单质既不是电解质,也不属于非电解质,故B正确;
C.二氧化碳溶于水能够导电,但是导电的离子不是二氧化碳电离的,所以二氧化碳为非电解质,故C正确;
D.硫酸钡的水溶液几乎不导电,但是硫酸钡在熔融状态下能够导电,硫酸钡所以电解质,且属于强电解质,故D错误;
故选BC.
点评:本题考查了电解质与非电解质的判断,题目难度不大,注意掌握电解质与非电解质的概念及判断方法,明确电解质、非电解质都一定为化合物,单质和混合物一定不属于电解质和非电解质.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
下列各组离子中,能在强酸性溶液里大量共存,并且溶液呈无色透明的是( )
| A、Cu2+、NO3-、Cl-、SO42- |
| B、Na+、K+、CO32-、Cl- |
| C、Mg2+、Na+、Cl-、NO3- |
| D、K+、Mg2+、ClO-、OH- |
下列实验操作中正确的是( )
| A、蒸发时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体也从下口放出 |
| D、过滤时,要用玻璃棒引流,并不断用玻璃棒搅拌,加快过滤速度 |
将标准状况下3.36L CO2缓慢通入1L 0.2mol?L-1的NaOH溶液中,气体被充分吸收,下列关系不正确的是( )
| A、c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| B、3c(Na+)=4[c (H2CO3)+c(HCO3-)+c(CO32-)] |
| C、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、3c(OH-)+2 c(CO32-)=c(HCO3-)+4c(H2CO3)+3c(H+) |
由乙炔、苯、乙二醇组成的混合物,经测定其中碳元素的质量分数为60%,则氢的质量分数为( )
| A、8.9% | B、35% |
| C、3.9% | D、5% |
将相同质量的铜分别与过量浓硝酸、稀硝酸在试管中反应,下列叙述正确的是( )
| A、在常温下,开始的反应速率:两者相同 |
| B、最终消耗硝酸的物质的量:前者多,后者少 |
| C、试管中气体的颜色:前者浅,后者深 |
| D、转移的电子总数:前者多,后者少 |
下列说法正确的是( )
| A、乙烷中混有杂质乙烯,用酸性高锰酸钾溶液出去乙烯 |
| B、1-丁烯存在顺反异构 |
| C、苯酚与氯化铁溶液的显色反应是物理变化 |
| D、甲烷与氯气光照会生成四种有机物 |
下列反应不属于取代反应的是( )
| A、苯酚溶液中加浓溴水. |
| B、乙醇和乙酸发生酯化反应 |
| C、乙醛催化氧化成乙酸 |
| D、乙醇分子间脱水 |
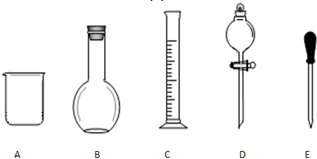 实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.