题目内容
将相同质量的铜分别与过量浓硝酸、稀硝酸在试管中反应,下列叙述正确的是( )
| A、在常温下,开始的反应速率:两者相同 |
| B、最终消耗硝酸的物质的量:前者多,后者少 |
| C、试管中气体的颜色:前者浅,后者深 |
| D、转移的电子总数:前者多,后者少 |
考点:硝酸的化学性质
专题:化学实验与化学计算
分析:A.反应速率与离子浓度成正比;
B.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,根据Cu的量计算消耗硝酸的量;
C.NO2是红棕色气体、NO是无色气体;
D.消耗铜的质量相等,则转移电子相等.
B.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,根据Cu的量计算消耗硝酸的量;
C.NO2是红棕色气体、NO是无色气体;
D.消耗铜的质量相等,则转移电子相等.
解答:
解:A.反应速率与离子浓度成正比,所以在常温下,开始的反应速率:前者大于后者,故A错误;
B.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,铜的质量相等,根据方程式知,浓硝酸消耗的量大于稀硝酸,故B正确;
C.NO2是红棕色气体、NO是无色气体,所以试管中气体的颜色:前者深,后者浅,故C错误;
D.消耗铜的质量相等,且铜都生成二价铜离子,所以转移电子相等,故D错误;
故选B.
B.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,铜的质量相等,根据方程式知,浓硝酸消耗的量大于稀硝酸,故B正确;
C.NO2是红棕色气体、NO是无色气体,所以试管中气体的颜色:前者深,后者浅,故C错误;
D.消耗铜的质量相等,且铜都生成二价铜离子,所以转移电子相等,故D错误;
故选B.
点评:本题考查了硝酸的性质,涉及反应速率、反应物的量、气体颜色等知识点,根据浓度与反应速率的关系结合方程式、气体的颜色等知识点来分析解答,题目难度不大.

练习册系列答案
相关题目
向含有下列离子的水溶液中,加入一小块金属钠,引起离子数目减少的是( )
| A、CO32- |
| B、OH- |
| C、HCO3- |
| D、Cu2+ |
下列关于平衡常数(K)的说法中正确的是( )
| A、相同温度下,不同浓度的同一弱电解质,其电离平衡常数(K)不同 | ||
| B、相同温度下,水的离子积常数就是水的电离平衡常数 | ||
C、由K水解=
| ||
| D、同温同浓度条件下,一元弱酸的电离平衡常数(K)越小,则溶液的pH越小 |
下列叙述正确的是( )
| A、熔融NaCl可以导电,则其溶液是电解质 |
| B、O3既不是电解质又不是非电解质 |
| C、CO2溶于水能导电,但CO2是非电解质 |
| D、BaSO4几乎不导电,是非电解质 |
下列说法中不正确的是( )
| A、干冰升华要吸收大量的热,但不是化学反应中的吸热反应 |
| B、酒精常被用做酒精灯和内燃机的燃料,说明酒精燃烧是放热反应 |
| C、人们用氢氧焰焊接或切割金属,主要是利用了氢气和氧气化合时放出的能量 |
| D、常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应 |
下列关于硝酸的说法中正确的是( )
| A、稀硝酸能与Fe发生反应,浓硝酸不能 |
| B、浓硝酸和稀硝酸都是强氧化剂 |
| C、稀硝酸是弱酸,浓硝酸是强酸 |
| D、稀硝酸与Cu反应生成NO,而浓硝酸与Cu反应生成NO2,稀硝酸得电子更多,故稀硝酸的氧化性大于浓硝酸 |
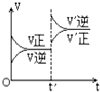 对达到平衡状态的可逆反应:X(?)+Y(?)?W(?)+Z(?)(已配平),在t'时增大压强,则正逆反应速率变化如右图所示(V代表速率,t代表时间.下列有关X、Y、Z、W的状态叙述正确的是( )
对达到平衡状态的可逆反应:X(?)+Y(?)?W(?)+Z(?)(已配平),在t'时增大压强,则正逆反应速率变化如右图所示(V代表速率,t代表时间.下列有关X、Y、Z、W的状态叙述正确的是( )| A、X、Y、W为气体,Z不是气体 |
| B、X、Y为气体,W、Z中有一种是气体 |
| C、W、Z为气体,X、Y中有一种是气体 |
| D、W、Z中有一种为气体,X、Y都不是气体 |
下列关于化学键的说法正确的( )
| A、只存在于分子之间 |
| B、相邻原子间强烈的相互作用 |
| C、只存在于离子之间、 |
| D、相邻分子间的相互作用 |
下列叙述正确的是( )
| A、离子化合物中必须含有金属阳离子 |
| B、物质中化学键被破坏,则一定发生化学变化 |
| C、NaCl的结构式为Na-Cl |
| D、H2O的沸点高于H2S |