题目内容
有一个装有CuCl2的烧杯,2根石墨电极,一根锌电极,铁电极和导线,设计个实验判断正负极.
考点:电解原理
专题:电化学专题
分析:根据锌电极,铁电极活性不同的两个电极、CuCl2溶液及形成闭合回路来构成原电池,活泼金属溶解作负极,在正极上析出铜来解答.
解答:
解:电极材料为锌电极,铁电极,电解质溶液为CuCl2溶液,用导线将锌电极,铁电极两个电极相连形成的原电池如图为 ,
,
活泼金属锌溶解作负极,正极上铁析出铜,可观察到有红色铜析出;
答: ,观察构成的原电池装置,有红色铜析出的一极的金属活泼性弱为正极,另一极锌溶解活泼性强为负极.
,观察构成的原电池装置,有红色铜析出的一极的金属活泼性弱为正极,另一极锌溶解活泼性强为负极.
 ,
,活泼金属锌溶解作负极,正极上铁析出铜,可观察到有红色铜析出;
答:
 ,观察构成的原电池装置,有红色铜析出的一极的金属活泼性弱为正极,另一极锌溶解活泼性强为负极.
,观察构成的原电池装置,有红色铜析出的一极的金属活泼性弱为正极,另一极锌溶解活泼性强为负极.
点评:本题考查了原电池的设计,原电池的设计关键是负极材料和电解质溶液的成分确定,侧重于考查原电池原理的应用,题目难度中等.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
下列关于“16g氧气”的叙述中,错误的是( )
| A、物质的量为0.5mol |
| B、气体体积为11.2L |
| C、含有NA 个氧原子 |
| D、含有8 NA个电子 |
保险丝是由武德合金制成的,武的合金是用50%铋、25%的铅、12.5%锡和12.5%的镉制成的,武德合金用于电器业主要是利用武德合金的( )
| A、熔点 | B、硬度 |
| C、稳定性 | D、导电性 |
 如图是氨基乙酸的球棍模型(图中的“棍”可能是单键,也可能是双键),该分子由四种元素的原子构成,它们原子半径的大小顺序是:X>Y>Z>W.
如图是氨基乙酸的球棍模型(图中的“棍”可能是单键,也可能是双键),该分子由四种元素的原子构成,它们原子半径的大小顺序是:X>Y>Z>W.
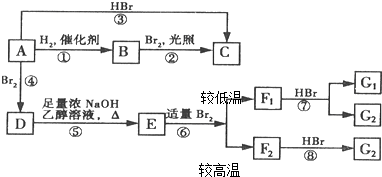
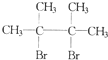 F1和F2为同分异构体,G1和G2互为同分异构体)
F1和F2为同分异构体,G1和G2互为同分异构体)