题目内容
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述中正确的是( )
| A、化学反应速率的关系是2v正(NH3)=3v正(H2O) |
| B、当4v正(O2)=5v逆(NO)时,该反应达到化学平衡状态 |
| C、若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| D、达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率增大 |
考点:化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到平衡时,反应速率之比等于化学计量数之比,并且正逆反应速率相等.
解答:
解:A、化学反应中反应速率之比等于化学计量数之比,根据化学方程式可知3v正(NH3)=2v正(H2O)成立,故A错误;
B、化学反应中反应速率之比等于化学计量数之比,根据化学方程式可知4v正(O2)=5v逆(NO),故B正确;
C、若单位时间内生成xmolNO的同时,消耗xmolNH3,则只表明反应正向进行,不能体现正逆反应速率相等,故C错误;
D、达到化学平衡时,若增加容器体积,则物质的浓度减小,正逆反应速率均减小,故D错误;
故选B.
B、化学反应中反应速率之比等于化学计量数之比,根据化学方程式可知4v正(O2)=5v逆(NO),故B正确;
C、若单位时间内生成xmolNO的同时,消耗xmolNH3,则只表明反应正向进行,不能体现正逆反应速率相等,故C错误;
D、达到化学平衡时,若增加容器体积,则物质的浓度减小,正逆反应速率均减小,故D错误;
故选B.
点评:本题考查化学平衡问题,题目难度不大,本题中注意平衡状态的判断、化学反应速率之比的等于化学计量数之比的利用以及可逆反应的特点.

练习册系列答案
相关题目
下列颜色变化不是因化学反应引起的是( )
| A、湿润的淀粉碘化钾试纸遇氯气变蓝 |
| B、鸡皮遇稀硝酸呈黄色 |
| C、蔗糖遇浓硫酸变黑 |
| D、钠燃烧时火焰呈黄色 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02 NA |
| B、标准状况下,0.5 mol/LBaCl2溶液中含有Cl-离子数为NA |
| C、通常状况下,NA个CO2分子占有的体积为22.4L |
| D、2.7g铝与盐酸完全反应失去0.2NA个电子 |
乙炔分子中碳原子的杂化类型为( )
| A、sp杂化 |
| B、sp2杂化 |
| C、sp3杂化 |
| D、都不是 |
下列说法正确的是( )
| A、由于氧化性HNO3大于H2SO4,所以非金属性:氮大于硫 |
| B、科学家在金属和非金属交界线处寻找催化剂 |
| C、只有主族元素是由短周期和长周期元素共同构成的 |
| D、长周期主族元素X的阳离子X2+的最外层有2个电子,则它是IVA族元素 |
在一密闭容器中,N2、H2合成氨的反应已达到平衡.此时再往容器中通入一定量N2气体,保持温度和容器体积不变,当反应再次达到平衡时,与第一次平衡状态相比( )
| A、NH3的百分含量增大 |
| B、NH3的浓度增大 |
| C、H2的转化率不变 |
| D、N2的转化率提高 |
已知维生素A的结构简式可写为 ,式中以线表示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H未标出来.关于它的叙述正确的( )
,式中以线表示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H未标出来.关于它的叙述正确的( )
 ,式中以线表示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H未标出来.关于它的叙述正确的( )
,式中以线表示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H未标出来.关于它的叙述正确的( )| A、维生素A的分子式为C20H30O |
| B、维生素A是一种易溶于水的醇 |
| C、维生素A的分子中有苯环结构并能使酸性高锰酸钾溶液褪色 |
| D、1 mol维生素A在催化剂的作用下最多可与5 mol H2发生加成反应 |
已知在2.2g某气体中所含的分子数目约为3.01×1022,此气体的摩尔质量为( )
| A、22g |
| B、22g/mol |
| C、44mol |
| D、44g/mol |
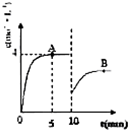 在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为:
在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为: