题目内容
5.下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )| A. | 150mL 1mol/L NaCl 溶液 | B. | 75mL 2mol/L CaCl2溶液 | ||
| C. | 150mL 2mol/L KCl 溶液 | D. | 75mL 1mol/L AlCl3溶液 |
分析 根据同一化学式中各微粒的浓度等于物质的物质的量浓度×离子个数,与溶液的体积无关,如50mL 1mol•L-1 MgCl2溶液中氯离子浓度为:n(Cl-)=1mol/L×2=2mol/L.
解答 解:50mL 1mol•L-1 MgCl2溶液中的Cl-的物质的量浓度为:c(Cl-)=2c(MgCl2)=2mol•L-1,
A、150mL 1mol•L-1 NaCl溶液中Cl-的物质的量浓度为:c(Cl-)=c(NaCl)=1mol•L-1,故A错误;
B、75mL 2mol•L-1CaCl2溶液中Cl-的物质的量浓度为:c(Cl-)=2c(CaCl2)=4mol•L-1,故B错误;
C、150mL 2mol•L-1 KCl溶液中Cl-的物质的量浓度为:c(Cl-)=c(KCl)=2mol•L-1,故C正确;
D、75mL 1mol•L-1AlCl3溶液中Cl-的物质的量浓度为:c(Cl-)=3c(AlCl3)=3mol•L-1,故D错误;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,试题侧重基础知识的考查,注意掌握物质的量浓度的概念及计算方法,明确物质的量浓度与溶液体积大小无关.

练习册系列答案
相关题目
16.1919年,科学家实现了人类多年的梦想--人工转变元素.这个核反应如下:$\stackrel{14}{7}$N+$\stackrel{4}{2}$He→${\;}_{8}^{17}$O+$\stackrel{1}{1}$H,下列有关叙述正确的是( )
| A. | ${\;}_{8}^{17}$O原子核内有9个质子 | |
| B. | $\stackrel{1}{1}$H原子核内有1个中子 | |
| C. | O2和O3互为同位素 | |
| D. | 通常情况下,He和N2化学性质都稳定 |
13.下列关于聚丙烯酸酯(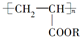 )的说法中,不正确的是( )
)的说法中,不正确的是( )
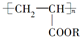 )的说法中,不正确的是( )
)的说法中,不正确的是( )| A. | 合成它的小分子化合物是CH3-CH2-COOR | |
| B. | 它可由CH2═CH-COOR经过加成聚合反应而得到 | |
| C. | 在一定条件下能发生水解反应 | |
| D. | 不能发生加成反应 |
10.下列离子方程式不正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| B. | 氨水中通入过量SO2:NH3•H2O+SO2═HSO3-+NH4+ | |
| C. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
14.运用有关概念判断下列说法中不正确的是( )
①BaSO4的水溶液不易导电,故BaSO4是弱电解质
②同位素的性质几乎完全相同
③利用Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥互称同位素的两种核素间具有相同的中子数和核外电子数.
①BaSO4的水溶液不易导电,故BaSO4是弱电解质
②同位素的性质几乎完全相同
③利用Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥互称同位素的两种核素间具有相同的中子数和核外电子数.
| A. | ①②④⑤ | B. | ③④⑤⑥ | C. | ②③⑤⑥ | D. | ①②⑤⑥ |
10.在一密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g)?N2(g)+2CO2(g);△H=-373.2kJ/mol,达到平衡后,为提高NO的转化率,采取的正确措施是( )
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |