题目内容
15.设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有( )①0.2mol H2O2完全分解转移的电子数为0.4NA
②25℃、101kPa下,16g O3和O2混合气体中含有的氧原子数为NA
③将含0.1mol FeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1molFe溶于过量稀硝酸,电子转移数为3NA
⑤标准状况下,22.4L CHCl3中含有的氯原子的数目为3NA.
| A. | ①②③ | B. | ①②④⑤ | C. | ①②③④ | D. | ②④ |
分析 ①H2O2分解为歧化反应;
②O3和O2均由氧原子构成;
③一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
④铁和过量稀硝酸反应后变为+3价;
⑤标准状况下,CHCl3为液态.
解答 解:①H2O2分解为歧化反应,1mol双氧水分解转移1mol电子,故0.2mol双氧水转移0.2NA个电子,故①错误;
②O3和O2均由氧原子构成,故16g氧气和臭氧的混合物中含有的氧原子的物质的量为1mol,即为NA个,故②正确;
③一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故故0.1mol氯化铁形成的胶粒的个数小于0.1NA个,故③错误;
④铁和过量稀硝酸反应后变为+3价,故1mol铁转移3NA个电子,故④正确;
⑤标准状况下,CHCl3为液态,故不能根据气体摩尔体积来计算其物质的量和含有的氯原子个数,故⑤错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
9.一种塑料抗氧化剂C可通过下列反应合成:
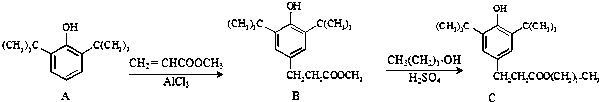
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 物质A中所有碳原子有可能位于同一平面 | |
| B. | 物质B可与4molH2发生加成反应 | |
| C. | 用酸性KMnO4溶液鉴别抗氧化剂C中是否含有CH3(CH2)17OH | |
| D. | B生成C的反应类型为取代反应 |
6.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 常温下0.1 mol/L的下列溶液①NH4Al(SO4)2、②NH4Cl、③NH3•H2O、④CH3COONH4溶液中,c(NH4+)由大到小的顺序是②>①>④>③ | |
| B. | 常温下0.4 mol/L CH3COOH溶液和0.2 mol/L NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度大小顺序为:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 0.1 mol/L(NH4)2Fe(SO4)2溶液:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol/L | |
| D. | 室温下,向0.1 mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
10.化学与人类生活、社会可持续发展密切相关.下列措施有利于节能减排、保护环境的是( )
①加快化石燃料的开采与使用②研发易降解的生物农药
③应用高效洁净的能源转换技术④田间焚烧秸秆
⑤推广使用节能环保材料.
①加快化石燃料的开采与使用②研发易降解的生物农药
③应用高效洁净的能源转换技术④田间焚烧秸秆
⑤推广使用节能环保材料.
| A. | ①③⑤ | B. | ②③⑤ | C. | ①②④ | D. | ②④ |
20.糖类、蛋白质是基本的营养物质,在我们的生活中扮演着及其重要的角色.如何识别这些物质的真伪,既可以检验同学们将化学知识与实际相结合的能力水平,又可以减少伪劣物品对我们生活质量的负面影响.请根据下列的实验现象填写表:
①烧焦羽毛味;②蓝色;③银镜(析出银);④砖红色沉淀;⑤黄色;
①烧焦羽毛味;②蓝色;③银镜(析出银);④砖红色沉淀;⑤黄色;
| 被鉴别的物质 | 鉴别物质(或鉴别方法) | 现象(填入序号即可) |
| 葡萄糖 | 新制氢氧化铜 | ④ |
| 淀粉 | 碘水 | ② |
| 蛋白质 | 浓硝酸 | ⑤ |
| 蛋白质 | 燃烧 | ① |
| 葡萄糖 | 银氨溶液 | ③ |
7.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1 L 0.1 mol•L-1 CuSO4溶液中含有0.1NA个Cu 2+ | |
| B. | 50 mL 18.4 mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 12 g石墨烯(单层石墨)中含有C-C的个数为1.5NA | |
| D. | 孤对电子对数均为NA的H2S和H2O在标准状况下占有体积相同 |
4.服药(片剂)时,应选用下列哪种物质送服( )
| A. | .茶水 | B. | 白开水 | C. | 啤酒 | D. | 饮料 |
5.下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150mL 1mol/L NaCl 溶液 | B. | 75mL 2mol/L CaCl2溶液 | ||
| C. | 150mL 2mol/L KCl 溶液 | D. | 75mL 1mol/L AlCl3溶液 |