题目内容
9.某烯烃(只含1个双键)与H2加成后的产物是 ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 先判断该烃结构是否对称,如果对称,只考虑该分子一边的结构和对称线两边相邻碳原子即可;如果不对称,要全部考虑,然后各去掉相邻碳原子上的一个氢原子形成双键.
解答 解:该烷烃的碳链结构为 ,1号和6号碳原子关于2号碳原子对称,5、8、9号碳原子关于4号碳原子对称,但4号碳原子上没有氢原子,所以4号碳原子和3、5、8、9号碳原子间不能形成双键;相邻碳原子之间各去掉1个氢原子形成双键,所以能形成双键有:1和2之间(或2和6);2和3之间;3和7之间,共有3种,
,1号和6号碳原子关于2号碳原子对称,5、8、9号碳原子关于4号碳原子对称,但4号碳原子上没有氢原子,所以4号碳原子和3、5、8、9号碳原子间不能形成双键;相邻碳原子之间各去掉1个氢原子形成双键,所以能形成双键有:1和2之间(或2和6);2和3之间;3和7之间,共有3种,
故选C.
点评 本题考查同分异构体的书写,分析分子结构是否对称是解本题的关键,注意不能重写、漏写,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.科学家预测原子序数为114的元素,它的位置在第7周期IVA族,称为类铅.关于它的性质,预测错误的是( )
| A. | 它的最外层电子数为4 | B. | 它的金属性比铅强 | ||
| C. | 它具有+2、+4价 | D. | 它的最高价氧化物的水化物是强酸 |
20.下列物质互为同分异构体的是( )
| A. | CH3COOH和CH3COOCH3 | B. | CH3CH2OH 和CH3OCH3 | ||
| C. | CH3OCHO和HCOOCH3 | D. | 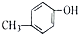 和 和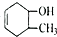 |
4.往NaOH溶液中加入少量的稀醋酸,若温度不变,下列数据一定增大的是( )
| A. | 溶液的导电性 | B. | 水的离子积 | C. | 离子总数 | D. | 溶液pH值 |
1.已知Y元素最高正价与最低负价的绝对值之差是4,Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
| A. | KCl | B. | K2S | C. | Na2S | D. | Na2O |
18.世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“至少在距今3000年以前,中国就已经使用玻璃了.”下列关于玻璃的叙述中,正确的是( )
| A. | 玻璃是人类最早使用的硅酸盐材料 | |
| B. | 玻璃在加热熔化时有固定的熔点 | |
| C. | 制造普通玻璃的原料主要是纯碱、粘土和石英 | |
| D. | 普通玻璃生产中所涉及的两个主要反应均有CO2生成 |
19.下列物质的化学用语正确的是( )
| A. | NH4H 的电子式: | B. | 硝基苯的结构简式: | ||
| C. | 丙烯的实验式:CH2 | D. | 甲烷分子的比例模型: |
 ;
;