题目内容
1.下列说法正确的是( )| A. | 1g甲烷和1g氧气的原子数之比为5:1 | |
| B. | 同温同压下甲烷和氧气的密度之比为2:1 | |
| C. | 等物质的量的甲烷和氧气的质量之比为2:1 | |
| D. | 在标准状况下等质量的甲烷和氧气的体积之比为1:2 |
分析 A.根据n=$\frac{m}{M}$计算物质的量之比,结合分子式计算含有原子数目之比;
B.同温同压下气体的密度之比等于其相对分子质量之比;
C.根据m=nM计算判断;
D.根据n=$\frac{m}{M}$计算物质的量之比,同温同压下气体的体积之比等于其物质的量之比.
解答 解:A.根据n=$\frac{m}{M}$可知,1g甲烷和1g氧气的物质的量之比为32g/mol:16g/mol=2:1,二者含有原子数之比为5×2:1×2=5:1,故A正确;
B.同温同压下气体的密度之比等于其相对分子质量之比,则同温同压下甲烷和氧气的密度之比为16:32=1:2,故B错误;
C.根据m=nM可知,等物质的量的甲烷和氧气的质量之比为16g/mol:32g/mol=1:2,故C错误;
D.根据n=$\frac{m}{M}$可知,等质量的甲烷和氧气的物质的量之比为32g/mol:16g/mol=2:1,同温同压下二者体积之比为2:1,故D错误,
故选:A.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
11.将5g 的CO与H2的混合气体和足量的氧气充分反应后,在150℃时将混合气体通过足量的Na2O2固体,则Na2O2固体增加的质量为( )
| A. | 1.5g | B. | 3g | C. | 5g | D. | 无法确定 |
9.下列实验方法错误的是( )
| A. | 除去氯化钾中混有的KI:溶于水通入过量氯气,蒸发结晶 | |
| B. | 除去Na2CO3固体中混有的NaHCO3:加热至恒重 | |
| C. | 除去食盐中的泥沙:溶于水,过滤,滤液蒸发结晶 | |
| D. | 从溴水中提取溴单质:加入酒精萃取 |
16.下列说法正确的是( )
| A. | 含有盐酸的洁厕剂和含有次氯酸钠的消毒液混用可以增强洗涤和消毒的效果 | |
| B. | 过量的Fe和Cu在等物质的量的Cl2中燃烧,转移的电子数相等 | |
| C. | 等体积、等浓度的NH4Cl溶液和稀氨水中,所含NH4+的数目相等 | |
| D. | 等物质的量的过氧化钡(BaO2)和Ba(OH)2固体中,阴阳离子个数比均为2:1 |
6.下列化学用语书写正确的是( )
| A. | 乙烯的结构简式 CH2CH2 | |
| B. | 氯离子的结构示意图: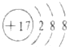 | |
| C. | H2O的电子式: | |
| D. | 碳酸钾的电离方程式 K2SO4=K2++SO42- |
10.下列不属于正在研究和开发的新能源是( )
| A. | 天然气 | B. | 生物质能 | C. | 氢能 | D. | 太阳能 |
3.分离混合物在工业生产中应用广泛.某含有金属钨(W)、WO2、WO3、W2O5的混合物,欲从该混合物中分离出WO3和W2O5,并冶炼金属钨,其流程示意图如所示.
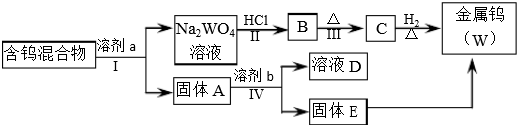
请阅读资料卡片并回答下列问题.
【资料卡片】
i.WO3易溶于NaOH、Na2CO3和Na2C2O4(草酸钠)溶液并形成钨酸盐(Na2WO4);W2O5易被氧化,也能溶解在上述溶液中;金属钨和WO2不溶于上述溶液.
ii.WO3几乎不与无机酸反应.
iii.钨化合物在不同溶剂中的浸取率见下表(浸取是用溶剂溶解固体混合物,以分离可溶性组分及残渣的过程.若浸取率为100%,则固体中的可溶组分全部溶解在溶剂中).
(1)步骤Ⅰ和Ⅳ均要进行的操作是过滤.
(2)步骤Ⅱ、Ⅲ反应的化学方程式分别是Na2WO4+2HCl=H2WO4+2NaCl、H2WO4$\frac{\underline{\;\;△\;\;}}{\;}$WO3+H2O.
(3)WO3既属于金属氧化物,也属于酸性氧化物,与NaOH溶液反应的离子方程式是WO3+2OH-=WO42-+H2O.
(4)步骤Ⅰ是将WO3分离出来,选用的试剂a是⑤,理由是将WO3溶解同时又能保证不被氧化W2O5.
(5)步骤Ⅳ可将W2O5分离出来,选用的试剂b是50g/L Na2CO3溶液,固体E中含有的物质是W、WO2,D中溶质是Na2WO4.

请阅读资料卡片并回答下列问题.
【资料卡片】
i.WO3易溶于NaOH、Na2CO3和Na2C2O4(草酸钠)溶液并形成钨酸盐(Na2WO4);W2O5易被氧化,也能溶解在上述溶液中;金属钨和WO2不溶于上述溶液.
ii.WO3几乎不与无机酸反应.
iii.钨化合物在不同溶剂中的浸取率见下表(浸取是用溶剂溶解固体混合物,以分离可溶性组分及残渣的过程.若浸取率为100%,则固体中的可溶组分全部溶解在溶剂中).
| 溶剂 | 煮沸时间(min) | W2O5(%) | WO3(%) | WO2 | 金属钨 |
| ①100g/L NaOH ②300g/LNa2CO3 ③50g/L Na2CO3 ④饱和Na2C2O4 ⑤饱和Na2C2O4(在CO2气氛下浸取) | 25 7 30 60 120 | 72.3 76.4 100 4.2 <0.5 | 100 100 100 100 100 | 未检出 | 未检出 |
(2)步骤Ⅱ、Ⅲ反应的化学方程式分别是Na2WO4+2HCl=H2WO4+2NaCl、H2WO4$\frac{\underline{\;\;△\;\;}}{\;}$WO3+H2O.
(3)WO3既属于金属氧化物,也属于酸性氧化物,与NaOH溶液反应的离子方程式是WO3+2OH-=WO42-+H2O.
(4)步骤Ⅰ是将WO3分离出来,选用的试剂a是⑤,理由是将WO3溶解同时又能保证不被氧化W2O5.
(5)步骤Ⅳ可将W2O5分离出来,选用的试剂b是50g/L Na2CO3溶液,固体E中含有的物质是W、WO2,D中溶质是Na2WO4.
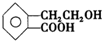 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.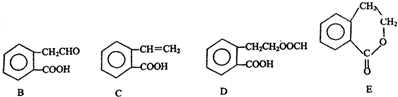
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O.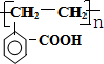 .
.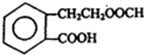 +2NaOH$\stackrel{△}{→}$HCOONa+
+2NaOH$\stackrel{△}{→}$HCOONa+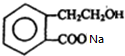 +2H2O.
+2H2O.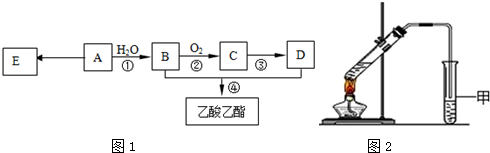
 .
.