题目内容
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器 .
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
MnO4-+ H2O2+ H+→ Mn2++ H2O+
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 .
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 (填“偏高”“偏低”“不变”).
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)请将他们所选的实验试剂和实验现象填入下表:
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)请将他们所选的实验试剂和实验现象填入下表:
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | ||
| 探究不稳定性 |
考点:中和滴定,氧化还原反应方程式的配平,过氧化氢,性质实验方案的设计
专题:实验设计题
分析:Ⅰ.(1)配制一定物质的量浓度的溶液需要容量瓶、滴定管;
(2)残缺方程式配平首先确定缺什么,根据电子转移守恒,配平化学方程式;
(3)滴定终点的现象是:滴入一滴高锰酸钾溶液,溶液呈红色,且半分钟内不褪色;
(4)根据化学方程式计算消耗过氧化氢的量然后计算质量分数;
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则有一部分溶液占据了气泡的体积.
II.如果双氧水能使淀粉碘化钾溶液变蓝色,则证明双氧水有氧化性;
如果将双氧水加热产生能使带火星的木条复燃的物质,则证明双氧水不稳定.
(2)残缺方程式配平首先确定缺什么,根据电子转移守恒,配平化学方程式;
(3)滴定终点的现象是:滴入一滴高锰酸钾溶液,溶液呈红色,且半分钟内不褪色;
(4)根据化学方程式计算消耗过氧化氢的量然后计算质量分数;
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则有一部分溶液占据了气泡的体积.
II.如果双氧水能使淀粉碘化钾溶液变蓝色,则证明双氧水有氧化性;
如果将双氧水加热产生能使带火星的木条复燃的物质,则证明双氧水不稳定.
解答:
解:Ⅰ.(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL,需要用到滴定管量取浓溶液的体积,配制溶液需要250mL容量瓶,
故答案为:滴定管、250mL容量瓶;
(2)方程式中,高锰酸钾有强氧化性,能将双氧水氧化为氧气,先确定缺的是O2,锰元素化合价降低了5价,生成1mol氧气时,氧元素化合价升高2价,根据电子转移守恒,配平化学方程式高锰酸根前面的系数为2,双氧水前面的系数为5,根据原子守恒来配平其他物质前面的系数,
故答案为:2;5;6;2;8;502;
(3)滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅紫色,且30秒内不褪色,故答案为:溶液由无色变为浅紫色且半分钟内不褪色;
(4)根据化学方程式可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol,则原过氧化氢的质量为:0.025cVmol×34g/mol=0.85cV,过氧化氢溶液中过氧化氢的质量分数为:
=
,故答案为:
;
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高,故答案为:偏高;
Ⅱ.如果双氧水能使淀粉碘化钾溶液变蓝色,则说明双氧水氧化碘离子生成碘单质,碘遇淀粉变蓝色,所以能证明双氧水有氧化性;
如果将双氧水加热产生能使带火星的木条复燃的物质,则说明双氧水分解生成氧气,所以能证明双氧水不稳定,
故答案为:
故答案为:滴定管、250mL容量瓶;
(2)方程式中,高锰酸钾有强氧化性,能将双氧水氧化为氧气,先确定缺的是O2,锰元素化合价降低了5价,生成1mol氧气时,氧元素化合价升高2价,根据电子转移守恒,配平化学方程式高锰酸根前面的系数为2,双氧水前面的系数为5,根据原子守恒来配平其他物质前面的系数,
故答案为:2;5;6;2;8;502;
(3)滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅紫色,且30秒内不褪色,故答案为:溶液由无色变为浅紫色且半分钟内不褪色;
(4)根据化学方程式可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol,则原过氧化氢的质量为:0.025cVmol×34g/mol=0.85cV,过氧化氢溶液中过氧化氢的质量分数为:
| 0.85cV |
| 10.00mL×ρg/mL |
| 0.085cV |
| ρ |
| 0.085cV |
| ρ |
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高,故答案为:偏高;
Ⅱ.如果双氧水能使淀粉碘化钾溶液变蓝色,则说明双氧水氧化碘离子生成碘单质,碘遇淀粉变蓝色,所以能证明双氧水有氧化性;
如果将双氧水加热产生能使带火星的木条复燃的物质,则说明双氧水分解生成氧气,所以能证明双氧水不稳定,
故答案为:
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | 淀粉碘化钾溶液 | 溶液变蓝 |
| 探究不稳定性 | 二氧化锰 | 产生能使带火星的木条变蓝的气体 |
点评:本题是一道综合知识题目,考查角度广,要求学生具有分析和解决问题的能力,难度大.

练习册系列答案
相关题目
一定温度,可逆反应2NO2?2NO+O2在体积固定的密闭容器中反应,达到平衡状态标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变 ⑥混合气体的平均摩尔质量不再改变.
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变 ⑥混合气体的平均摩尔质量不再改变.
| A、①④⑤⑥ | B、①②③⑤ |
| C、②③④⑥ | D、以上全部 |
下列有关实验的叙述正确的是( )
| A、除去水中的Na+、SO42-、Cl-等杂质可用蒸馏的方法 |
| B、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
| C、用铂丝蘸取少量某溶液进行焰色反应,若火焰呈黄色,则原溶液含有钠盐 |
| D、某溶液加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液含有SO42- |
能鉴别MgSO4、A1C13、K2CO3、NH4Cl四瓶溶液的一种试剂是( )
| A、AgNO3溶液 |
| B、盐酸 |
| C、NaOH溶液 |
| D、氨水 |
某物质的化学式为PtCl4?2NH3,其水溶液不导电,加入AgNO3溶液不产生沉淀,加入强碱也没有NH3放出,则关于此化合物的说法中正确的是( )
| A、该配合物中中心原子(离子)的电荷数和配位数均为6 |
| B、该配合物可能是平面正方形结构 |
| C、Cl- 和NH3分子均与中心原子(离子)形成配位键 |
| D、配合物中心原子(离子)与Cl-形成配位键,而与NH3分子不形成配位键 |
最近,科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是( )
| A、在冷的浓H2SO4溶液中可钝化 |
| B、在潮湿的空气中放置不易生锈 |
| C、熔点比钢高 |
| D、硬度比生铁大 |

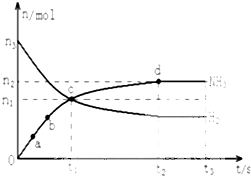 氨气主要用作致冷剂及制取铵盐和氨肥
氨气主要用作致冷剂及制取铵盐和氨肥