题目内容
下列表明化学方程式中电子转移的方向和数目正确的是( )
A、 |
B、 |
C、 |
D、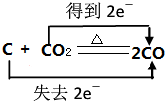 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:化合价升高的元素的原子失去电子,失去多少电子化合价就升高几价;化合价降低的元素的原子得到电子,得到多少电子化合价就降低几价.氧化还原反应中得失电子数目相等.
解答:
解:A.反应中Cu元素化合价由+2价降低到0价,应得到电子,故A错误;
B.反应中P元素化合价由0价升高到+5价,被氧化,应失去电子,为还原剂,而O元素化合价由0价降低到-2价,被还原,为氧化剂,得电子,故B错误;
C.反应中Mn元素化合价由+4价降低到+2价,转移电子数目错误,应为2,故C错误;
D.反应中只有C元素化合价变化,分别由0价、+4价变化为+2价,故D正确.
故选D.
B.反应中P元素化合价由0价升高到+5价,被氧化,应失去电子,为还原剂,而O元素化合价由0价降低到-2价,被还原,为氧化剂,得电子,故B错误;
C.反应中Mn元素化合价由+4价降低到+2价,转移电子数目错误,应为2,故C错误;
D.反应中只有C元素化合价变化,分别由0价、+4价变化为+2价,故D正确.
故选D.
点评:本题考查氧化还原反应的电子转移,侧重于学生的分析能力的考查,为高频考点,难度中等,根据判断准化合价变化以及变化的原子数目.

练习册系列答案
相关题目
下列各组气体中均能造成大气污染的是( )
| A、CO2、O2 |
| B、N2、NO |
| C、NO2、SO2 |
| D、Cl2、N2 |
下列能用勒沙特列原理解释的是( )
①H2(g)+I2(g)?2HI(g)平衡后增大压强颜色变深
②Fe(SCN)3溶液中加入固体KSCN后颜色变深
③物质的量浓度相同的NH4HSO4溶液和CH3COONH4溶液,c(NH4+)前者大
④乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利
⑤向AgCl悬浊液中加入KI溶液有黄色沉淀生成.
①H2(g)+I2(g)?2HI(g)平衡后增大压强颜色变深
②Fe(SCN)3溶液中加入固体KSCN后颜色变深
③物质的量浓度相同的NH4HSO4溶液和CH3COONH4溶液,c(NH4+)前者大
④乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利
⑤向AgCl悬浊液中加入KI溶液有黄色沉淀生成.
| A、②③④⑤ | B、①②④ |
| C、①③⑤ | D、全部 |
异戊烷的二氯代物的同分异构体共有( )
| A、7种 | B、8种 | C、9种 | D、10种 |
为了说明醋酸是弱电解质,某同学设计了如下实验方案证明,其中错误的是( )
| A、配制0.10 mol/L CH3COOH溶液,测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 |
| B、用pH计分别测0.01 mol/L和0.10 mol/L的醋酸溶液的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质 |
| C、对盐酸和醋酸溶液进行导电性实验,若与CH3COOH溶液相串联的灯泡较暗,证明醋酸为弱电解质 |
| D、配制0.10 mol/L CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质 |
银锌电池是广泛用做各种电子仪器的电源,其放电过程可表示为Ag2O+Zn═ZnO+2Ag,此电池放电时,负极上发生反应的物质是( )
| A、Ag |
| B、ZnO |
| C、Ag2O |
| D、Zn |
如图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
| A | C | |
| B |
| A、B为第二周期的元素 |
| B、C为VA族元素 |
| C、三种元素都为非金属元素 |
| D、C是稀有气体元素 |
下列药品的保存方法正确的是( )
| A、少量金属钠保存在水中 |
| B、烧碱溶液保存在带玻璃塞的磨口玻璃试剂瓶中 |
| C、新制氯水保存在棕色细口试剂瓶中 |
| D、漂白粉盛装在细口玻璃试剂瓶中 |
下列物质中,互为同分异构体是( )
| A、HCOOCH3和乙酸 |
| B、麦芽糖和纤维素 |
| C、HCOOH和 乙醇 |
| D、蔗糖和果糖 |