题目内容
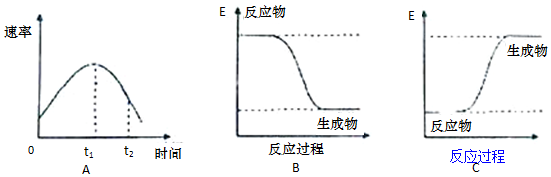
4.某小组同学在烧杯中加入5mL1.0mol•L-1盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是放热(填“吸热”或“放热”)反应,其能量变化可用图中的B(填“B”或“C”)表示.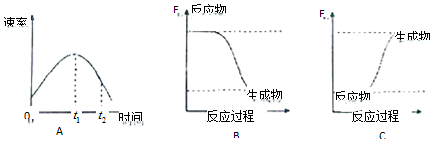
分析 浓度越小,反应速率越小,温度越高,速率越大;放热反应中,反应物的总能量大于生成物的总能量,吸热反应中,反应物的总能量小于生成物的总能量.
解答 解:在烧杯中加入5mL 1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,开始时盐酸的浓度减小,速率应减小,但实际上增大,说明温度对速率的影响大于浓度对速率的影响,则该反应放热;放热反应中,反应物的总能量大于生成物的总能量,则图象B正确,
故答案为:放热;B.
点评 本题考查反应热与焓变的应用,为高频考点,侧重于学生的分析能力的考查,主要把握反应的特点,解题的关键是分析实验的过程,并结合题中所给的信息结合所学相关知识对问题进行探讨与分析.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
14.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 乙酸和乳酸(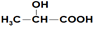 )的混合物共3.0 g,含有的原子总数为0.4 NA )的混合物共3.0 g,含有的原子总数为0.4 NA | |
| B. | 4.6 g乙醇含有-OH数为NA | |
| C. | 1.7 g H2O2中含有的电子数为NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
15.铜锌原电池的装置如图所示,下列说法正确的是( )
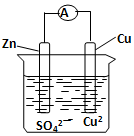

| A. | 锌电极上发生还原反应 | B. | 铜电极上发生氧化反应 | ||
| C. | 铜片上都有氧气产生 | D. | 电流由铜流向锌 |
12.下列物质可用铁制容器盛装的是( )
| A. | 亚硫酸 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 胆矾溶液 |
9.下列化合物均为天然萜类化合物:
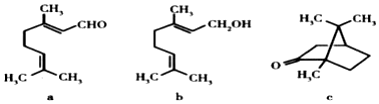
对这些萜类化合物叙述错误的是( )

对这些萜类化合物叙述错误的是( )
| A. | 三种化合物中只有a 和c 互为同分异构体 | |
| B. | 一定条件下a 和b可相互转化 | |
| C. | 三种化合物均易被氧化 | |
| D. | 三种化合物均可催化氢化 |
13.短周期元素的性质递变规律如图所示,下列说法正确的是( )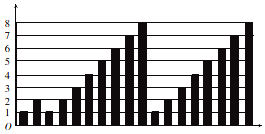

| A. | 横坐标为质子数,纵坐标为元素的最高正价 | |
| B. | 横坐标为原子序数,纵坐标为元素原子的最外层电子数 | |
| C. | 横坐标为核电荷数,纵坐标为元素原子的半径 | |
| D. | 横坐标为中子数,纵坐标为元素的非金属性 |