题目内容
在一定条件下,某密闭容器中发生反应:
2SO2(g)+O2(g)![]() 2SO3(g)+Q,反应达到平衡后,SO2,O2,SO3的物质的量之比为3∶2∶4.其他条件不变,升高温度达到新的平衡时,n(SO2)=1.4mol,n(O2)=0.9mol,则此时SO3物质的量为
2SO3(g)+Q,反应达到平衡后,SO2,O2,SO3的物质的量之比为3∶2∶4.其他条件不变,升高温度达到新的平衡时,n(SO2)=1.4mol,n(O2)=0.9mol,则此时SO3物质的量为
[ ]
|
A.1.4mol |
B.1.6mol |
|
C.1.8mol |
D.2.0mol |
答案:B
解析:
解析:
|
导解:新平衡时 n(SO2)∶n(O2)=1.4∶0.9>3∶2说明升高温度平衡逆向移动.设旧平衡时SO2,O2,SO3物质的量分别为3a mol,2a mol,4a mol,升高温度有x mol SO3反应.2SO2+O2  2SO3 2SO3
旧平衡 (mol) 3a 2a 4a转化 (mol) x x/2 x新平衡 (mol) 3a+x 2a+ 4a-x 4a-x

则 SO3为4×0.4-0.2=1.6mol. |

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
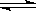 2SO3(g) , △H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为( )。
2SO3(g) , △H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为( )。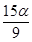 mol B.
mol B. mol C.
mol C.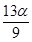 mol D.
mol D.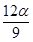 mol
mol 2SO3(g) △H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( )
2SO3(g) △H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( )