题目内容
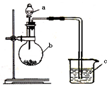 已知:元素最高价氧化物对应的水化物酸性越强,元素原子的得电子能力越强.某化学兴趣小组同学为了验证硫与碳的得电子能力的强弱,用如图所示装置设计实验.根据要求回答问题:
已知:元素最高价氧化物对应的水化物酸性越强,元素原子的得电子能力越强.某化学兴趣小组同学为了验证硫与碳的得电子能力的强弱,用如图所示装置设计实验.根据要求回答问题:(1)仪器a应盛放的药品是
A.H2SO4 B.H2SO3 C.H2S D.H2CO3
(2)仪器b应盛放的药品是
A.Na2SO4 B.Na2CO3 C.NaCl D.CaCO3
(3)仪器c盛放的药品是
考点:实验装置综合,非金属在元素周期表中的位置及其性质递变的规律
专题:实验设计题
分析:比较非金属性的强弱,可根据最高价氧化物的水化物的酸性强弱比较,本题可用稀硫酸与碳酸钠反应验证,C中为澄清石灰水,如变浑浊,则说明生成二氧化碳,可证明硫与碳的得电子能力的强弱,以此解答该题.
解答:
解:(1)比较非金属性的强弱,可根据最高价氧化物的水化物的酸性强弱比较,可用稀硫酸与碳酸盐反应进行验证,故答案为:A;
(2)仪器b中为碳酸钠,不能用碳酸钙,因生成硫酸钙微溶于水,阻碍反应的继续进行,故答案为:B;
(3)C中为澄清石灰水,如变浑浊,则说明生成二氧化碳,可证明硫比碳的得电子能力的强,
故答案为:澄清石灰水;c中澄清石灰水变浑浊;硫;碳.
(2)仪器b中为碳酸钠,不能用碳酸钙,因生成硫酸钙微溶于水,阻碍反应的继续进行,故答案为:B;
(3)C中为澄清石灰水,如变浑浊,则说明生成二氧化碳,可证明硫比碳的得电子能力的强,
故答案为:澄清石灰水;c中澄清石灰水变浑浊;硫;碳.
点评:本题通过实验的方法来考查元素周期律的有关知识,为高频考点,侧重于学生的分析能力和实验能力的考查,设计角度新颖,能较好地考查学生的综合解题能力,难度不大.

练习册系列答案
相关题目
下列各项操作,错误的是( )
| A、用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 |
| B、进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出 |
| C、萃取、分液前需对分液漏斗进行检漏 |
| D、将玻璃塞上的凹槽对准漏斗口颈上的小孔,可以保证分液漏斗内的液体顺利流出 |
 在5-氨基四唑(
在5-氨基四唑( )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊. 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.
