题目内容
【题目】叠氮化钠(NaN3)是制备医药、炸药的一种重要原料,采用“亚硝酸甲酯-水合肼法”制备叠氮化钠的生产流程如下:
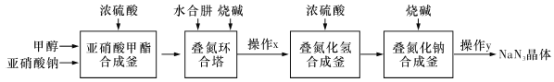
回答下列问题:
(1)亚硝酸甲酯合成釜中生成的亚硝酸甲酯(CH3ONO)易转化为气态进入叠氮环合塔,写出生成CH3ONO的化学反应方程式:_________________________________________________。
(2)叠氮环合塔中生成叠氮化钠的过程中生成一可循环使用的有机物,其官能团电子式为___________,该合成过程的化学方程式为______________________________________。
(3)已知氨基、氨气因有孤对电子而呈现一定碱性,所以水合肼(N2H4·H2O)的性质类似一水合氨,将硫酸与水合肼反应可以生成酸式盐,该盐的化学式为___________;叠氮环合塔中滴加的烧碱溶液要适当过量,目的主要是_________________________________。
A.促进NaN3水解 B抑制NaN3水解 C.作催化剂且对NaN3水解无影响
(4)生产中有HN3生成,请设计实验证明HN3为弱酸:________________________________。
(5)化工生产中,多余的NaN3常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理13 g NaN3,理论上需加入0.5 mol·L-1的NaClO溶液___________mL。
【答案】2CH3OH+2NaNO2+H2SO4=2CH3ONO+Na2SO4+2H2O ![]() N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O (N2H6)(HSO4)2 B 使用pH试纸测定NaN3溶液的酸碱性,若该溶液显碱性,说明HN3为弱酸(也可采用其他方法,如测定0.1 mol·L-1HN3的pH,若pH大于1,说明HN3为弱酸) 200
N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O (N2H6)(HSO4)2 B 使用pH试纸测定NaN3溶液的酸碱性,若该溶液显碱性,说明HN3为弱酸(也可采用其他方法,如测定0.1 mol·L-1HN3的pH,若pH大于1,说明HN3为弱酸) 200
【解析】
NaNO2与甲醇、浓硫酸反应得到CH3ONO,加入NaOH、水合肼溶液反应:CH3ONO+N2H4·H2O+NaOH═CH3OH+NaN3+3H2O,得到NaN3,加热、浓缩,加入浓硫酸,得到(N2H6)(HSO4)2,加入氢氧化钠,蒸馏将甲醇分离,结晶、抽滤、洗涤、干燥得到产品。
(1)亚硝酸甲酯合成釜中生成的亚硝酸甲酯(CH3ONO)易转化为气态进入叠氮环合塔,浓硫酸、甲醇和亚硝酸钠,浓硫酸可以酸化亚硝酸钠,并为酯化反应提供催化剂,得到甲醇的无机酸酯和水,方程式为2CH3OH+2NaNO2+H2SO4=2CH3ONO+Na2SO4+2H2O,故答案为:2CH3OH+2NaNO2+H2SO4=2CH3ONO+Na2SO4+2H2O;
(2)由于在亚硝酸甲酯合成釜里形成了酯,在叠氮环合塔中酯又水解,因此整个过程中甲醇是可以循环利用的,-OH电子式为![]() ,叠氮环合塔中加入了水合肼与烧碱,烧碱可以使第一步得到的亚硝酸甲酯水解,产生甲醇和亚硝酸钠,同时亚硝酸钠和肼里的氮元素发生归中反应得到产物叠氮化钠,方程式为N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O,
,叠氮环合塔中加入了水合肼与烧碱,烧碱可以使第一步得到的亚硝酸甲酯水解,产生甲醇和亚硝酸钠,同时亚硝酸钠和肼里的氮元素发生归中反应得到产物叠氮化钠,方程式为N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O,
故答案为:![]() ;N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O;
;N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O;
(3)既然水合肼的性质类似一水合氨,在水中应该能电离产生N2H62+和OH-,因此它的硫酸酸式盐的化学式为(N2H6)(HSO4)2;叠氮环合塔中适当滴加过量的烧碱有两个作用,一方面可以提高亚硝酸甲酯和水合肼的转化率,另一方面可以抑制叠氮化钠这个强碱弱酸盐的水解,故选B;
故答案为:(N2H6)(HSO4)2;B;
(4)若要证明HN3为弱酸,可以用pH试纸来检测NaN3溶液的pH,根据“有弱就水解”的规则,若溶液显碱性,则证明HN3为弱酸,其它合理的方法也可以,如测定0.1 mol·L-1HN3的pH,若pH大于1,说明HN3为弱酸,
故答案为:使用pH试纸测定NaN3溶液的酸碱性,若该溶液显碱性,说明HN3为弱酸(也可采用其他方法,如测定0.1 mol·L-1HN3的pH,若pH大于1,说明HN3为弱酸);
(5)根据描述,NaN3应该被氧化为无毒的N2.同时ClO-被还原为Cl-,因此每个NaN3在反应中需要失去1个电子,每个ClO-在反应中可以得到2个电子,二者的物质的量之比为2:1;NaN3的物质的量n=![]() =0.1mol,则需要ClO-的物质的量为0.10mol,因此需要次氯酸钠溶液体积V=
=0.1mol,则需要ClO-的物质的量为0.10mol,因此需要次氯酸钠溶液体积V=![]() =0.2L=200mL,
=0.2L=200mL,
故答案为:200。

 阅读快车系列答案
阅读快车系列答案【题目】用图所示装置检验乙烯时不需要除杂的是

乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |