��Ŀ����
9��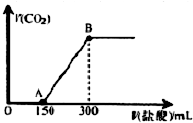 ���������3mol/L��NaOH��Һ500mL�������NaOH����60.0g��
���������3mol/L��NaOH��Һ500mL�������NaOH����60.0g����1���ڸ���Һ�����ƹ����У��õ��IJ���������500mL����ƿ����ͷ�ιܡ���Ͳ���ձ�����������
��2������ڶ���ʱ���ӣ���ҺŨ�Ƚ�ƫС��������ʱҺ����ڿ̶���Ӧ��ȡ�Ĵ�ʩ���������ƣ�
��ȡ����ʵ�������Ƶ�NaOH��Һ100mL������ͨ��һ������CO2����ַ�Ӧ����������Һ�ʼ��ԣ�
��1����ʱ��Һ���������ǵ�һ�ɷ֣�������Na2CO3��NaHCO3��
��2������������������Һ�У���λ����μ�1mol/L�����ᣬ�����������������������������������ܽ���ˮ����ϵ��ͼ��ʾ��
����ͼ��֪��������Һ�еĵ�һ����ΪNa2CO3��
����д��0-A����������Ӧ�����ӷ���ʽCO32-+H+�THCO3-��
��B��ʱ��������CO2�ڱ�״���µ����Ϊ3360mL��B��ʱ����Ӧ������Һ�����ʵ����ʵ���Ũ����0.75mol/L��������Һ���ʱ�������ֱ����ӣ�
���� I������n=cV��m=nM�����㣻
��1���������Ʋ����Ǽ��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ��������Ҫ��������
��2������c=$\frac{n}{V}$��������ʵ����ʵ���n����Һ�����V�ı仯��������������
II����1��CO2��NaOH��Ӧ������Na2CO3��NaHCO3��������Һ���ʼ��ԣ�
��2����������1500mLʱ��ʼ�������壬����������300mLʱ���ٲ������壬O��A�η�����Ӧ��Na2CO3+HCl�TNaCl+NaHCO3��A��B�η���NaHCO3+HCl�TNaCl+H2O+CO2������O��A�����ĵ�����ΪA��B���ĵ�����Ķ�������
�ٸ���ͼ���֪�����������һ��ʼ���������ɣ��ʿ���֪��һ�����ʣ�
��O��A�η�����Ӧ��Na2CO3+HCl�TNaCl+NaHCO3��
�۸���AB�η�Ӧ��������B����Һ������ΪNaCl�����������غ��֪n��NaCl��=n��NaOH�������������Ȼ��Ƶ�Ũ�ȣ�
��� �⣺I������3mol/L��NaOH��Һ500mL��������������Ƶ����ʵ���n=cV=3mol/L��0.5L=1.5mol������m=nM=1.5mol��40g/mol=60.0g���ʴ�Ϊ��60.0��
��1���������Ʋ����Ǽ��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ��֪�����������500mL����ƿ�ͽ�ͷ�ιܡ���Ͳ���ձ������������ʴ�Ϊ��500mL����ƿ��
��2������ڶ���ʱ���ӣ�����Һ�����ƫ����ҺŨ�Ƚ�ƫС��������ʱҺ����ڿ̶���Ӧ��ȡ�Ĵ�ʩ���������ƣ��ʴ�Ϊ��ƫС���������ƣ�
II����1��CO2��NaOH��Ӧ������Na2CO3��NaHCO3��������Һ���ʼ��ԣ�������ǵ�һ�ɷ֣�������Na2CO3��NaHCO3��
�ʴ�Ϊ��Na2CO3��NaHCO3��
��2����������200mLʱ��ʼ�������壬����������300mLʱ���ٲ������壬�����������������������������������Ϊ1��1����֪��Һ�е�����ΪNa2CO3��O��A�η�����Ӧ��Na2CO3+HCl�TNaCl+NaHCO3��A��B�η���NaHCO3+HCl�TNaCl+H2O+CO2����
�ٸ���ͼ���֪����������200mLʱ��ʼ�������壬����������300mLʱ���ٲ������壬�����������������������������������Ϊ1��1����֪��Һ�е�����ΪNa2CO3���ʿ���֪��һ������ΪNa2CO3���ʴ�Ϊ��Na2CO3��
��O��A�η�����Ӧ��Na2CO3+HCl�TNaCl+NaHCO3�������ӷ���ʽΪ��CO32-+H+�THCO3-���ʴ�Ϊ��CO32-+H+�THCO3-��
��A��B�η���NaHCO3+HCl�TNaCl+H2O+CO2����������������Ϊ150mL�����ʵ���n=CV=1mol/L��0.15L=0.15mol�������ɵĶ�����̼�����ʵ���Ϊxmol�����У�
NaHCO3+HCl�TNaCl+H2O+CO2��
1 1
0.15mol xmol
����$\frac{1}{0.15mol}=\frac{1}{xmol}$
���x=0.15mol��
0.15mol������̼�ڱ���µ����V=nVm=0.15mol��22.4L/mol=3360mL��
B����Һ������ΪNaCl�����������غ��֪n��NaCl��=n��NaOH��=0.1L��3mol/L=0.3mol����NaCl�����ʵ���Ũ���ǣ�$\frac{0.3mol}{0.1L+0.3L}$=0.75mol/L��
�ʴ�Ϊ��3360mL��0.75mol/L��
���� ���⿼������ļ��㣬��Ŀ�Ѷ��еȣ��ؼ��Ǹ���ͼ��������η����ķ�Ӧ��ע�����������غ�˼���Ӧ�ã�

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�| A�� | �������Ǹ��ϲ��� | B�� | ���Ǻ�ɫ�������� | ||
| C�� | ʯӢ�ǰ뵼����� | D�� | ˮ�����������ǽ������� |
ʵ�飨һ�� �⺬���IJⶨ
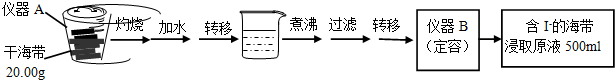
ȡ0.0100mol•L��1��AgNO3����Һװ��ζ��ܣ�ȡ100.00mL������ȡԭҺ���ζ��أ��õ��Ƶζ����ⶨ�⺬������ĵ綯�ƣ�E�� ��ӳ��Һ��c��I�����ı仯�������������±���
| V��AgNO3��/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
���ƺ�����ȡԭҺ���ס�������ʵ�鷽�����£�
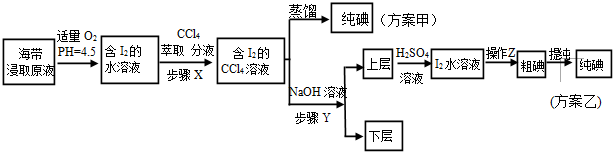
��֪��3I2+6NaOH�T5NaI+NaIO3+3H2O����ش�
��1��ʵ�飨һ�� �е��������ƣ�����A���������� B500mL����ƿ��
��2���ôεζ��յ�ʱ��ȥAgNO3��Һ�����Ϊ20.00mL������ú����е�İٷֺ���Ϊ0.635%��
��3���ٷ�Һ©��ʹ��ǰ���©��
�ڲ���X�У���ȡ���Һ©���ڹ۲쵽��������Һ���Ϊ�������㣬�²���Ϻ�ɫ��
�������йز���Y��˵������ȷ����AB��
A��Ӧ����NaOH��Һ��Ũ�Ⱥ���� B������ת�������ӽ���ˮ��
C����Ҫ�dz�ȥ������ȡԭҺ�е��л����� D��NaOH��Һ�������Ҵ�����
��4���������в����������������ǵⵥ�����������ᵼ�µ���ʧ��
| A�� | ��NaHSO4��Һ�еμ�Ba��OH��2��Һ�����ԣ�Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| B�� | ��Na2CO3��Һ��ͨ������CO2��2Na++CO32-+CO2+H2O�T2NaHCO3�� | |
| C�� | ��Ca��HCO3��2��Һ�м�������Ca��OH��2��Һ��Ca2++HCO3-+2OH-�TCaCO3��+CO32-+2H2O | |
| D�� | ���������Һ�еμ�NaOH��Һ��H++OH-�TH2O |
| A�� | �϶���SO2��NO��O2 | B�� | �϶�û��C12��O2��NO2 | ||
| C�� | ������Cl2��O2 | D�� | �϶�ֻ��NO |
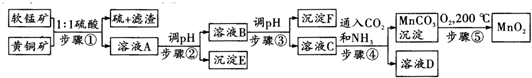
��֪����1������?5MnO2+2CuFeS2+10H2SO4�T5MnSO4+Fe2��SO4��3+2CuSO4+4S��+10H2O
?����������������������ʽ����ʱ��Һ��pH���±���
| ������ | Cu��OH��2 | Fe��OH��3 | Mn��OH��2 | Fe��OH��2 |
| ��ʼ����pH | 4.2 | 1.5 | 7.3 | 6.4 |
| ��ȫ����pH | 6.7 | 3.2 | 9.8 | 9.0 |
��1������?����ÿ����64g��ת�Ƶ��ӵ���ĿΪ5NA��
��2������?����pH�ķ�Χ��3.2��pH��4.2��3.2��pH��4.2������E��Ҫ�ɷֵĻ�ѧʽΪFe��OH��3��
��3��MnSO4��Һ��c��MnSO4��=3��10-6mol/L��ij̼������Һ��c��CO32-��=3.3��10-5mol/L��������Һ�������2��1��ϣ�ǡ�ôﵽ�ܽ�ƽ�⣬��MnCO3��Ksp=2.2��10-11��
��4������ܷ��������ӷ�Ӧ����ʽ��Mn2++2NH3+CO2+H2O=MnCO3��+2NH4+��
��5����ȡ0.58g���̿����ձ��У��ٷֱ����ձ��м������20.00mL0.1000mol/LNa2C2O4��Һ���������ᣬ��ֽ����ܽ⣬���ˣ�����Һת������ƿ�У���0.1000mol/L��KMnO4��Һ�ζ����յ㣬������4.00mLKMnO4��Һ���йط�Ӧ���£�
MnO2+Na2C2O4+2H2SO4�TMnSO4+Na2SO4+2CO2��+2H2O
5Na2C2O4+2KMnO4+8H2SO4�T2MnSO4+K2SO4+5Na2SO4+10CO2��+8H2O
��ʵ������У����ڵζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���ζ��ܼ��첿�ֲ��������ݣ����ʹ�ζ�ʱ���ĵ�KMnO4��Һ���ƫ���ƫ����ƫС�����䡱����
�ڼ������̿���MnO2 �İٷֺ�����15.0%��
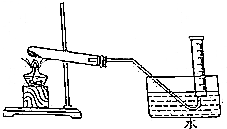 Ϊ��֤MnO2��KClO3���ȷֽ���O2�ķ�Ӧǰ���������䣬ij��ȤС��������ͼ��ʾװ�ý���������ʵ�飺
Ϊ��֤MnO2��KClO3���ȷֽ���O2�ķ�Ӧǰ���������䣬ij��ȤС��������ͼ��ʾװ�ý���������ʵ�飺