题目内容
请按要求填空:
(1)N元素基态原子的电子排布图为
(2)Fe2+的外围电子排布式为
(3)基态X原子有7个轨道填充了电子,则X元素价层电子排布式为
(4)33号元素的简化电子排布式 ,Cu元素的外围电子排布式 .
(1)N元素基态原子的电子排布图为
(2)Fe2+的外围电子排布式为
(3)基态X原子有7个轨道填充了电子,则X元素价层电子排布式为
(4)33号元素的简化电子排布式
考点:原子核外电子排布,原子核外电子的能级分布
专题:原子组成与结构专题
分析:(1)N原子核外有7个电子,分别位于1S、2S、2P轨道;
(2)Fe是26号元素,其原子核外有26个电子,铁原子失去2个电子生成Fe2+,其3d轨道上6个电子为其外围电子;
(3)基态X原子有7个轨道填充了电子,分别是1s、2s、2p、3s、3p轨道,且3p轨道有1个电子,为Al元素,其3s、3p电子为其价电子;
(4)33号元素是As元素,其原子核外有33个电子,根据构造原理书写其简化电子排布式;Cu原子核外有29个电子,其3d、4s电子为其外围电子.
(2)Fe是26号元素,其原子核外有26个电子,铁原子失去2个电子生成Fe2+,其3d轨道上6个电子为其外围电子;
(3)基态X原子有7个轨道填充了电子,分别是1s、2s、2p、3s、3p轨道,且3p轨道有1个电子,为Al元素,其3s、3p电子为其价电子;
(4)33号元素是As元素,其原子核外有33个电子,根据构造原理书写其简化电子排布式;Cu原子核外有29个电子,其3d、4s电子为其外围电子.
解答:
解:(1)N原子核外有7个电子,分别位于1S、2S、2P轨道,其轨道表示式为 ,故答案为:
,故答案为: ;
;
(2)Fe是26号元素,其原子核外有26个电子,铁原子失去2个电子生成Fe2+,其3d轨道上6个电子为其外围电子,其价电子排布式为3d6,故答案为:3d6;
(3)基态X原子有7个轨道填充了电子,分别是1s、2s、2p、3s、3p轨道,且3p轨道有1个电子,为Al元素,其3s、3p电子为其价电子,所以其价电子排布式为3s23p1,故答案为:3s23p1;
(4)33号元素是As元素,其原子核外有33个电子,根据构造原理知其简化电子排布式为[Ar]3d104s24p3;Cu原子核外有29个电子,其3d、4s电子为其外围电子,所以其外围电子排布式为3d104s1,故答案为:[Ar]3d104s24p3;3d104s1.
 ,故答案为:
,故答案为: ;
;(2)Fe是26号元素,其原子核外有26个电子,铁原子失去2个电子生成Fe2+,其3d轨道上6个电子为其外围电子,其价电子排布式为3d6,故答案为:3d6;
(3)基态X原子有7个轨道填充了电子,分别是1s、2s、2p、3s、3p轨道,且3p轨道有1个电子,为Al元素,其3s、3p电子为其价电子,所以其价电子排布式为3s23p1,故答案为:3s23p1;
(4)33号元素是As元素,其原子核外有33个电子,根据构造原理知其简化电子排布式为[Ar]3d104s24p3;Cu原子核外有29个电子,其3d、4s电子为其外围电子,所以其外围电子排布式为3d104s1,故答案为:[Ar]3d104s24p3;3d104s1.
点评:本题考查了原子核外电子排布式的书写,明确原子结构是解本题关键,再结合构造原理来书写即可,知道哪些电子是价电子,为易错点.

练习册系列答案
相关题目
某有机物的结构简式为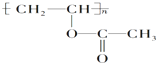 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A、1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1mol |
| B、该有机物水解所得产物能发生取代反应 |
| C、该有机物可通过加聚反应生成 |
| D、该有机物的单体只有一种且能使溴水褪色 |
根据热化学方程式:S(s)+O2(g)═SO2(g)△H=a kJ?mol-1(a=-297.2),下列说法中不正确的是( )
| A、S(s)在氧气中燃烧的反应是放热反应 |
| B、S(s)+O2(g)═SO2(g)△H=b kJ?mol-1,则a<b |
| C、1mol SO2(g)所具有的能量低于1mol S(s)与1mol O2(g)所具有的能量之和 |
| D、16g固体硫在氧气中充分燃烧,可放出148.6kJ的热量 |
常温下,物质的量浓度相同的三种盐NaX、NaY和NaZ溶液的pH依次为8、9、10,则下列表达式不正确的是( )
| A、Z-+H2O?HZ+OH- |
| B、HZ+Y-═HY+Z- |
| C、HY+H2O?H3O++Y- |
| D、HX+Z-═HZ+X- |
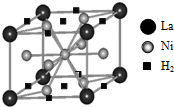 能源、材料和信息是现代社会的三大“支柱”.
能源、材料和信息是现代社会的三大“支柱”.