题目内容
下列说法正确的是( )
| A、常温下,反应4Na(s)+O2(g)═2Na2O(s)的△H<0,△S>0 | |||
| B、反应2A(g)+B(g)═3C(s)+D(g)在一定条件下能自发进行,说明该反应的△H<0 | |||
| C、合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |||
D、反应2SO2+O2
|
考点:反应热和焓变,化学平衡的影响因素
专题:
分析:A.Na与O2在常温下反应放热且反应后无气体生成,故△H<0,△S<0;
B.该反应在一定条件下能自发进行,根据△G=△H-T△S<0判断;
C.合成氨生产中将NH3液化分离,能使反应体系中NH3的浓度降低,虽然提高了反应物的转化率,但降低了反应速率;
D.升温,v(正)、v(逆)均增大.
B.该反应在一定条件下能自发进行,根据△G=△H-T△S<0判断;
C.合成氨生产中将NH3液化分离,能使反应体系中NH3的浓度降低,虽然提高了反应物的转化率,但降低了反应速率;
D.升温,v(正)、v(逆)均增大.
解答:
解:A.Na与O2在常温下反应放热且反应后无气体生成,故△H<0,△S<0,故A错误;
B.该反应在一定条件下能自发进行,△G=△H-T△S<0,则有△H<T△S,因△S<0,T>0,故有△H<0,故B正确;
C.合成氨生产中将NH3液化分离,能使反应体系中NH3的浓度降低,虽然提高了反应物的转化率,但降低了反应速率,故C错误;
D.升温,v(正)、v(逆)均增大,故D错误.
故选B.
B.该反应在一定条件下能自发进行,△G=△H-T△S<0,则有△H<T△S,因△S<0,T>0,故有△H<0,故B正确;
C.合成氨生产中将NH3液化分离,能使反应体系中NH3的浓度降低,虽然提高了反应物的转化率,但降低了反应速率,故C错误;
D.升温,v(正)、v(逆)均增大,故D错误.
故选B.
点评:本题考查焓变和熵变以及速率的影响因素,题目难度中等,注意△S的判断,反应能否自发进行,须满足△G=△H-T?△S<0.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在铁的吸氧腐蚀中,发生还原反应的电极上进行的电极反应是( )
| A、2 H++2e-═H2↑ |
| B、O2+2H2O+4e-═4OH- |
| C、Fe-2e-═Fe2+ |
| D、4 OH--4e-═2H2O+O2↑ |
下列反应中,是吸热反应的是( )
| A、铝片与稀硫酸反应 |
| B、Ba(OH)2?8H2O晶体与氯化铵晶体反应 |
| C、盐酸与氢氧化钠溶液反应 |
| D、乙醇在空气中燃烧 |
下列各组元素中按微粒半径递增顺序排列的是( )
| A、Li K Na |
| B、Ba2+ Ca2+ Mg2+ |
| C、Ca2+ K+ Cl- |
| D、N O F |
下列叙述正确的是( )
| A、O2的结构式为 O-O |
B、硫离子的结构示意图为: |
C、CCl4分子的比例模型: |
D、H2O的电子式: |

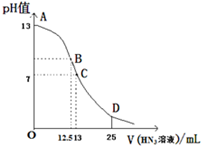 纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).
纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).
