题目内容
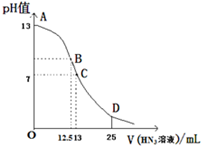 纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).
纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).①根据图象写出HN3的电离方程式
②D点时溶液中各离子浓度由大到小的顺序为
③若B点时溶液的pH=8,则溶液中c( HN3)=
考点:弱电解质在水溶液中的电离平衡,离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:①图象分析恰好反应时消耗HN3的体积为12.5ml,此时溶液PH为8显碱性,说明HN3为弱酸;
②D点加入25mlHN3溶液得到等浓度的NaN3和 HN3溶液,溶液PH小于7显酸性,说明酸电离大于水解;
③根据B点时氢氧化钠和HN3溶液恰好完全反应生成NaN3,根据NaN3溶液的电荷守恒和物料守恒来计算.
②D点加入25mlHN3溶液得到等浓度的NaN3和 HN3溶液,溶液PH小于7显酸性,说明酸电离大于水解;
③根据B点时氢氧化钠和HN3溶液恰好完全反应生成NaN3,根据NaN3溶液的电荷守恒和物料守恒来计算.
解答:
解:①图象分析氢氧化钠溶液和HN3溶液恰好反应时消耗HN3的体积为12.5ml,此时溶液PH为8显碱性,说明HN3为弱酸,电离方程式为:HN3?H++N3-,
故答案为:HN3?H++N3-;
②D点加入25mlHN3溶液得到等浓度的NaN3和 HN3溶液,溶液PH小于7显酸性,说明酸电离大于水解,溶液中离子浓度大小为C(N3-)>C(Na+)>C(H+)>C(OH-);
故答案为:C(N3-)>C(Na+)>C(H+)>C(OH-);
(3)B点时氢氧化钠和HN3溶液恰好完全反应生成NaN3,根据NaN3溶液的电荷守恒有:C(N3-)+C(OH-)=C(Na+)+C(H+) ①
由于氢氧化钠溶液与HN3溶液的体积已知,故溶液中C(Na+)可以求得 ②
由于溶液的pH=8,故C(H+)=10-8mol/L ③
C(OH-)=10-6mol/L ④
解①②③④可知C(N3-)=C(Na+)+10-8-10-6①
再根据物质守恒可知:C(N3-)+c(HN3)=C(Na+)②
解①②可得:c(HN3)=(10-6-10-8)mol/L
故答案为:10-6-10-8.
故答案为:HN3?H++N3-;
②D点加入25mlHN3溶液得到等浓度的NaN3和 HN3溶液,溶液PH小于7显酸性,说明酸电离大于水解,溶液中离子浓度大小为C(N3-)>C(Na+)>C(H+)>C(OH-);
故答案为:C(N3-)>C(Na+)>C(H+)>C(OH-);
(3)B点时氢氧化钠和HN3溶液恰好完全反应生成NaN3,根据NaN3溶液的电荷守恒有:C(N3-)+C(OH-)=C(Na+)+C(H+) ①
由于氢氧化钠溶液与HN3溶液的体积已知,故溶液中C(Na+)可以求得 ②
由于溶液的pH=8,故C(H+)=10-8mol/L ③
C(OH-)=10-6mol/L ④
解①②③④可知C(N3-)=C(Na+)+10-8-10-6①
再根据物质守恒可知:C(N3-)+c(HN3)=C(Na+)②
解①②可得:c(HN3)=(10-6-10-8)mol/L
故答案为:10-6-10-8.
点评:本题考查了弱电解质的电离方程式书写、离子浓度大小比较、离子浓度的计算,注意守恒思想的应用,掌握基础是关键,题目难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列物质中不能使品红溶液褪色的是( )
| A、次氯酸钠 | B、二氧化硫 |
| C、盐酸 | D、氯气 |
下列物质间的每步转化只需通过一步反应就能实现的是( )
| A、S→SO3→H2SO4→Na2SO3 |
| B、Al→Al(OH)3→Al2O3→NaAlO2 |
| C、Na→Na2O2→Na2CO3→NaOH |
| D、Si→SiO2→H2SiO3→Na2SiO3 |
CH3COONa稀溶液中分别加入少量下列物质或改变如下条件,能使比值
一定减小的是( )
①固体NaOH ②固体KOH ③固体NaHSO4④固体CH3COONa ⑤冰醋酸 ⑥降温.
| c(CH3COO-) |
| c(Na+) |
①固体NaOH ②固体KOH ③固体NaHSO4④固体CH3COONa ⑤冰醋酸 ⑥降温.
| A、只有①③ | B、①③④ |
| C、②④⑤⑥ | D、③④⑥ |
相同温度下,有下列三个热化学方程式:
(1)2H2(l)+O2(g)═2H2O(l)△H1=-Q1 kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(l)△H1=-Q2 kJ?mol-1
(3)2H2(l)+O2(g)═2H2O(g)△H1=-Q3 kJ?mol-1
则Q1、Q2、Q3的关系表示正确的是( )
(1)2H2(l)+O2(g)═2H2O(l)△H1=-Q1 kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(l)△H1=-Q2 kJ?mol-1
(3)2H2(l)+O2(g)═2H2O(g)△H1=-Q3 kJ?mol-1
则Q1、Q2、Q3的关系表示正确的是( )
| A、Q1=Q2<Q3 |
| B、Q2>Q1>Q3 |
| C、Q3>Q2>Q1 |
| D、Q1=Q2=Q3 |
下列说法正确的是( )
| A、常温下,反应4Na(s)+O2(g)═2Na2O(s)的△H<0,△S>0 | |||
| B、反应2A(g)+B(g)═3C(s)+D(g)在一定条件下能自发进行,说明该反应的△H<0 | |||
| C、合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |||
D、反应2SO2+O2
|
下列化学应用中不涉及氧化还原反应的是 ( )
| A、Na2S水溶液在空气中变浑浊 |
| B、生活中使用明矾净水,除去水中的悬浮颗粒 |
| C、溶有二氧化氮的浓硝酸做火箭的助燃剂 |
| D、漂白粉漂白有色布条 |
“绿色化学”提倡化工生产应尽可能将反应物的原子全部利用,从根本上解决环境污染问题.在下列制备环氧乙烷的反应中,最符合“绿色化学”思想的是( )
A、 |
| B、CH2=CH2+Cl2+Ca(OH)2→CH2-CH2+CaCl2+H2O |
C、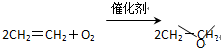 |
D、 |