题目内容
4.下列说法正确的是( )| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 在化合物Na2O2中,阴、阳离子的个数比为1:1 | |
| C. | 在化合物CaCl2中,两个氯离子之间存在共价键 | |
| D. | 液态HCl不能导电,属于共价化合物 |
分析 A.离子键就是使阴阳离子结合成化合物的静电作用;
B.过氧化钠中过氧根离子显-2价,晶体中阴阳离子个数比为1:2;
C.在化合物CaCl2中,氯离子和钙离子之间存在离子键,两个氯离子之间没有共价键;
D.液态HCl不能导电.
解答 解:A.离子键就是使阴阳离子结合成化合物的静电作用,静电作用包含吸引力和排斥力,故A错误;
B.过氧化钠中过氧根离子显-2价,其电子式是 ,晶体中阴阳离子个数比为1:2,故B错误;
,晶体中阴阳离子个数比为1:2,故B错误;
C.CaCl2是离子化合物,由钙离子与氯离子构成,电子式为 ,两个氯离子之间没有共价键,故C错误;
,两个氯离子之间没有共价键,故C错误;
D.液态HCl不能导电,属于共价化合物,故D正确;
故选D.
点评 本题考查共价键与离子键、离子化合物与共价化合物的区别,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
14.已知丁基有4种结构,分子式为C5H10O2的羧酸有( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
15.下列叙述正确的是( )
①热稳定性:H2O>HF>H2S
②泥水、淀粉溶液、盐酸分别属于悬浊液、胶体、溶液
③ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤第IA族元素铯的两种同位素137Cs比133Cs多4个质子
⑥已知2H2(g)+O2(g)=2H2O(l)△H=-571kJ•mol-1则氢气的燃烧热为△H=-285.5kJ•mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
①热稳定性:H2O>HF>H2S
②泥水、淀粉溶液、盐酸分别属于悬浊液、胶体、溶液
③ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤第IA族元素铯的两种同位素137Cs比133Cs多4个质子
⑥已知2H2(g)+O2(g)=2H2O(l)△H=-571kJ•mol-1则氢气的燃烧热为△H=-285.5kJ•mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
| A. | 只有②④⑥ | B. | 只有①⑤⑥ | C. | 只有②③④ | D. | 只有③⑤⑦ |
9.某有机物的蒸汽完全燃烧时需三倍于其体积的氧气,产生二倍于其体积的二氧化碳该有机物可能是( )
| A. | C2H6 | B. | C2H5OH | C. | C2H4O | D. | C2H4O2 |
13.已知:
①1mol H2分子中化学键断裂时需要吸收436KJ的能量
②1 mol Cl2分子中化学键断裂时需要吸收243 kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431 kJ的能量
对于反应:H2(g)+Cl2(g)═2HCl(g),下列叙述正确的是( )
①1mol H2分子中化学键断裂时需要吸收436KJ的能量
②1 mol Cl2分子中化学键断裂时需要吸收243 kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431 kJ的能量
对于反应:H2(g)+Cl2(g)═2HCl(g),下列叙述正确的是( )
| A. | 反应生成2mol氯化氢气体,吸收248KJ的能量 | |
| B. | 反应生成2mol氯化氢气体,放出183KJ的能量 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 该反应为吸热反应 |
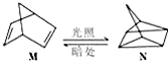 △H=+88.6kJ/mol
△H=+88.6kJ/mol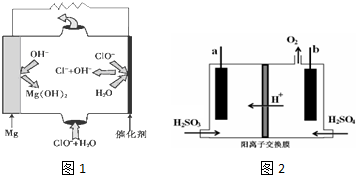
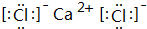 ;
; .
. 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.
能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.