题目内容
19.将锌片和铜片按如图方式插入柠檬中,电流计指针发生偏转.则下列说法中正确的是( )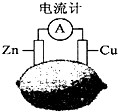
| A. | 该装制能将电能转换为化学能 | B. | 电子由铜片流出经导线到锌片 | ||
| C. | 一段时间后,锌片质量减轻 | D. | 铜片一侧产生Cu2+使柠檬变蓝色 |
分析 锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,以此解答.
解答 解:A.该装置是将化学能转化为电能的装置,为原电池,故A错误;
B.电子从负极锌流向正极铜,故B错误;
C.锌易失电子作负极,锌失电子变成锌离子,锌片质量减轻,故C正确;
D.铜片上电极方程式为2H++2e-=H2↑,故D错误;
故选C.
点评 本题考查了原电池原理,明确原电池和电解池的判断方法,再结合金属失电子的难易程度确定正负极,电子的移动方向,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
7.下列有关说法正确的是( )
| A. | H2、SO2、CO2三种气体都可用浓硫酸干燥 | |
| B. | Fe(OH)3胶体为无色、透明,能发生丁达尔现象 | |
| C. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| D. | SiO2既能和氢氟酸反应又能和氢氧化钠溶液反应,所以是两性氧化物 |
14.向盛有FeCl3溶液的试管中滴入KSCN溶液,溶液呈( )
| A. | 无色 | B. | 红色 | C. | 蓝色 | D. | 浅绿色 |
11.下列说法不正确的是( )
| A. | 配制一定物质的量浓度的硫酸溶液时,定容时俯视会造成溶液浓度偏高 | |
| B. | 量取15.20mL AgNO3溶液可以用酸式滴定管 | |
| C. | 过滤完毕,洗涤沉淀时应该向漏斗中加水至没过沉淀,用玻璃棒搅拌充分洗剂,重复2~3次 | |
| D. | 蒸发浓缩CuSO4溶液时,要用玻璃棒搅拌防止溶液溅出 |
8.某工厂废水中含有毒的CrO42-和Cr2O72-,常见处理方法是使其转化为毒性较低的Cr3+或直接吸附除去.现有如下几种工艺:
(1)光催化法:在催化剂作用下,利用太阳光和人工光,使废水实现上述转化.
①该法的反应原理是2Cr2O72-+16H+→4Cr3++3O2+8H2O(将方程式补充完整)
②该法涉及的能量转化形式是.
③某小组通过实验研究催化剂中W(钨)和α-Fe2O3的比例对铬的去除率的影响(每次实验均采用:0.01mol/L 500mL酸化的K2Cr2O7溶液、总质量为0.2g的催化剂、光照10min),六价铬的去除率如下表所示.
上表中,b=15%;在去除率最高的催化剂实验组中,用Cr2O72-表示的该反应在10min内的平均化学反应速率v=mol/(L•min).
(2)电化学处理法:向废铁屑(铁碳合金)中加入含铬废水,一段时间后,废水中六价铬元素的去除率能达到90%.
①废铁屑在使用前酸洗除锈的离子方程式是Fe2O3+6H+=2Fe3++3H2O.
②结合电化学原理说明废铁屑在此过程中所起的作用是铁在原电池反应中做负极Fe-2e-=Fe2+,Fe2+做还原剂将六价铬还原.
(3)离子交换树脂(ROH)法:将CrO42-和Cr2O72-吸附至树脂上除去,原理如下:
2ROH+CrO42-→R2CrO4+2OH-、2ROH+Cr2O72-→R2Cr2O7+2OH-
(已知:废水中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O).
控制溶液酸性可以提高树脂对六价铬的去除率,其理由是由原理可知:2ROH~CrO42-~Cr,2ROH~Cr2O72-~2Cr,等量树脂去除Cr2O72-的效率高,因此控制酸性使上述平衡正向移动,使CrO42-转化为Cr2O72-.
(1)光催化法:在催化剂作用下,利用太阳光和人工光,使废水实现上述转化.
①该法的反应原理是2Cr2O72-+16H+→4Cr3++3O2+8H2O(将方程式补充完整)
②该法涉及的能量转化形式是.
③某小组通过实验研究催化剂中W(钨)和α-Fe2O3的比例对铬的去除率的影响(每次实验均采用:0.01mol/L 500mL酸化的K2Cr2O7溶液、总质量为0.2g的催化剂、光照10min),六价铬的去除率如下表所示.
| 催化剂组成 | 1 | 2 | 3 |
| WO3 W α-Fe2O3 | 65% 5% 30% | 65% 10% 25% | a b 20% |
| 六价铬去除率 | 60.2% | 80% | 72.9% |
(2)电化学处理法:向废铁屑(铁碳合金)中加入含铬废水,一段时间后,废水中六价铬元素的去除率能达到90%.
①废铁屑在使用前酸洗除锈的离子方程式是Fe2O3+6H+=2Fe3++3H2O.
②结合电化学原理说明废铁屑在此过程中所起的作用是铁在原电池反应中做负极Fe-2e-=Fe2+,Fe2+做还原剂将六价铬还原.
(3)离子交换树脂(ROH)法:将CrO42-和Cr2O72-吸附至树脂上除去,原理如下:
2ROH+CrO42-→R2CrO4+2OH-、2ROH+Cr2O72-→R2Cr2O7+2OH-
(已知:废水中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O).
控制溶液酸性可以提高树脂对六价铬的去除率,其理由是由原理可知:2ROH~CrO42-~Cr,2ROH~Cr2O72-~2Cr,等量树脂去除Cr2O72-的效率高,因此控制酸性使上述平衡正向移动,使CrO42-转化为Cr2O72-.
9.往氯水中滴入Na2SO3溶液的pH变化如图所示,下列说法正确的是( )
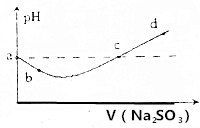

| A. | a点表示的溶液中存在3种分子,3种离子 | |
| B. | b点溶液中不存在SO2 | |
| C. | c点溶液中c(Na+)=2c(HSO3-)+2c(SO32-) | |
| D. | d点溶液中不存在HSO3- |
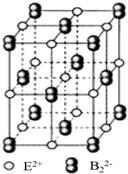 原子序数小于36的A、B、C、D、E五种元素,原子序数依次增大,A、D能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1,B是形成化合物种类最多的元素,C原子基态时2p原子轨道上有3个未成对的电子,E基态原子的第一能层与第四能层填充的电子数相同,第二能层与第三能层填充的电子数相同.
原子序数小于36的A、B、C、D、E五种元素,原子序数依次增大,A、D能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1,B是形成化合物种类最多的元素,C原子基态时2p原子轨道上有3个未成对的电子,E基态原子的第一能层与第四能层填充的电子数相同,第二能层与第三能层填充的电子数相同.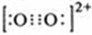 ;1mol D22+中含有的π键数目为2NA.
;1mol D22+中含有的π键数目为2NA.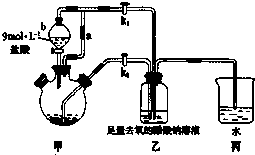 醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种为红棕色晶体,极易被氧气氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂).
醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种为红棕色晶体,极易被氧气氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂). 为探究生活中两种常见的有机物的性质,某同学设计如下实验,请根据题目要求回答下列问题:
为探究生活中两种常见的有机物的性质,某同学设计如下实验,请根据题目要求回答下列问题: