题目内容
已知反应:①A2+2B-=2A-+B2②B2+2C-=2B-+C2③C2+2D-=2C-+D2,则A-、B-、C-、D-还原性的正确顺序是( )
| A、A->B->C->D- |
| B、D->C->B->A- |
| C、A->D->B->C- |
| D、D->B->A->C- |
考点:氧化性、还原性强弱的比较
专题:
分析:氧化还原反应中氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物,标注反应过程中元素化合价变化分析判断氧化剂、还原剂、还原产物、氧化产物,利用规律分析判断.
解答:
解:①A2+2B-=2A-+B2,反应中B元素化合价由-1价变化为0价,化合价升高做还原剂,A-为A2被还原的产物,故还原性B->A-;
②B2+2C-=2B-+C2,反应中C元素化合价-1价变化为0价,化合价升高做还原剂,得到的还原产物为2B-,还原性C->B-;
③同理分析得出:还原性D->C-;
综上所述还原性强弱顺序:D->C->B->A-;
故选B.
②B2+2C-=2B-+C2,反应中C元素化合价-1价变化为0价,化合价升高做还原剂,得到的还原产物为2B-,还原性C->B-;
③同理分析得出:还原性D->C-;
综上所述还原性强弱顺序:D->C->B->A-;
故选B.
点评:本题考查了氧化还原反应中氧化性和还原性的强弱比较方法和规律应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
100g浓度为c1的浓氨水(溶质质量分数为ω1)与Vml的谁混合,得浓度为c2的稀氨水(溶质质量分数为ω2),下列说法正确的是( )
| A、若ω1=2ω2,则c1<2c2,V=100ml |
| B、若ω1=2ω2,则c1>2c2,V=100ml |
| C、若c1=2c2,则ω1<2ω2,V>100ml |
| D、若c1=2c2,则,ω1=2ω2,V=100ml |
下列离子方程式正确的是( )
| A、铁和硝酸银溶液反应:Fe+Ag+=Ag+Fe3+ |
| B、氢氧化镁与硫酸溶液反应:H++OH-=H2O |
| C、碳酸钙与醋酸溶液反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
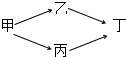 甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙.回答下列问题:
甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙.回答下列问题: