题目内容
15.同位素常用做环境分析指示物,下列对同位素的说法正确的是( )| A. | 34S原子核内的中子数为16 | B. | 13C和15N原子核内的质子数相差2 | ||
| C. | 16O与18O的核电荷数相等 | D. | 2H+质量与1H+的质量相同 |
分析 A.利用质子数+中子数=质量数来计算;
B.C原子的质子数为6,N原子的质子数为7;
C.16O与18O的质子数相等;
D.元素符号的左上角为质量数.
解答 解:A.34S原子核内的中子数为34-16=18,故A错误;
B.C原子的质子数为6,N原子的质子数为7,则13C和15N原子核内的质子数相差7-6=1,故B错误;
C.16O与18O的质子数相等,核电荷数相等,故C正确;
D.元素符号的左上角为质量数,分别为2、1,故D错误.
故选C.
点评 本题考查同位素及原子的构成等知识,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4 L氯水含有NA个Cl2分子 | |
| B. | 在1 L 0.1 mol•L-1碳酸钠溶液中阴离子总数大于0.1NA | |
| C. | 50 mL18.4 mol•L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 标准状况下,由H2O2制得4.48 LO2转移的电子数目为0.8NA |
10. M和N单质燃烧时均放出大量热,可用作燃料.已知M和N均为短周期元素,其原子的第一至第四电离能如下表所示:
M和N单质燃烧时均放出大量热,可用作燃料.已知M和N均为短周期元素,其原子的第一至第四电离能如下表所示:
根据上述信息,M的原子结构示意图为 ,MCl2是非极性(填“极性分子”或“非极性分子”);N的核外电子排布如图所示,该同学所画的电子排布图违背了能量最低原理.
,MCl2是非极性(填“极性分子”或“非极性分子”);N的核外电子排布如图所示,该同学所画的电子排布图违背了能量最低原理.
 M和N单质燃烧时均放出大量热,可用作燃料.已知M和N均为短周期元素,其原子的第一至第四电离能如下表所示:
M和N单质燃烧时均放出大量热,可用作燃料.已知M和N均为短周期元素,其原子的第一至第四电离能如下表所示:| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| M | 932 | 1821 | 15390 | 21771 |
| N | 738 | 1451 | 7733 | 10540 |
 ,MCl2是非极性(填“极性分子”或“非极性分子”);N的核外电子排布如图所示,该同学所画的电子排布图违背了能量最低原理.
,MCl2是非极性(填“极性分子”或“非极性分子”);N的核外电子排布如图所示,该同学所画的电子排布图违背了能量最低原理.
20.如图装置中(烧杯中均盛有海水),铁不易被腐蚀的是( )
| A. |  | B. | 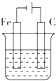 | C. |  | D. |  |
4.下列说法中正确的是( )
| A. | 能溶于水的盐是强电解质,不溶于水的盐是非电解质 | |
| B. | 强电解质溶液中不存在分子,弱电解质溶液中必存在溶质分子 | |
| C. | 在熔融状态下能导电的化合物一定是离子化合物,也一定是强电解质 | |
| D. | 强电解质一定能导电,非电解质的水溶液一定不导电 |
5.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,6.4g O2和O3的混合气体中含有的原子数为0.4NA | |
| B. | 在反应中消耗0.1molCl2,转移的电子数一定为0.2NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜粉完全反应,生成气体分子的数目为2NA | |
| D. | 标准状况下,11.2L CCl4中含有的分子数目为0.5NA |


 Al3++3HCO3-=Al(OH)3↓+3CO2↑.
Al3++3HCO3-=Al(OH)3↓+3CO2↑. Al(OH)3+3H+═Al3++3H2O.
Al(OH)3+3H+═Al3++3H2O.
 .
.