题目内容
5.用NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,6.4g O2和O3的混合气体中含有的原子数为0.4NA | |
| B. | 在反应中消耗0.1molCl2,转移的电子数一定为0.2NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜粉完全反应,生成气体分子的数目为2NA | |
| D. | 标准状况下,11.2L CCl4中含有的分子数目为0.5NA |
分析 A、氧气和臭氧均由氧原子构成;
B、根据氯气反应后的价态来分析;
C、铜只能与浓硫酸反应,与稀硫酸不反应;
D、标况下四氯化碳为液态.
解答 解:A、氧气和臭氧均由氧原子构成,故6.4g混合物中含有的氧原子的物质的量n=$\frac{6.4g}{16g/mol}$=0.4mol,个数为0.4NA个,故A正确;
B、由于氯气反应后的价态可能为-1价或+1价或+3价或+5价或+7价,故转移的电子数不一定是0.2NA个,故B错误;
C、铜只能与浓硫酸反应,与稀硫酸不反应,故2mol浓硫酸不能反应完全,则生成的气体分子小于NA个,故C错误;
D、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
15.同位素常用做环境分析指示物,下列对同位素的说法正确的是( )
| A. | 34S原子核内的中子数为16 | B. | 13C和15N原子核内的质子数相差2 | ||
| C. | 16O与18O的核电荷数相等 | D. | 2H+质量与1H+的质量相同 |
16.下列各组离子在给定条件下,一定能大量共存的是( )
| A. | 含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ | |
| B. | 在pH=12的溶液中:ClO-、SO32-、Na+、K+ | |
| C. | 能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COOO-、I- | |
| D. | 澄清透明的溶液中:Cu2+、Fe3+、NO3?、Cl ? |
13.下列反应的离子方程式不正确的是( )
| A. | 溴化亚铁溶液中通入过量氯气.2Fe2++2Br-+2C12═2Fe3++Br2+4C1- | |
| B. | 草酸和少量烧碱溶液:H2C2O4+OH-═HC2O4-+H2O | |
| C. | 漂白粉溶液吸收过量的二氧化碳:ClO-十H2O+CO2═HClO+HCO3- | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全NH4++H++SO42-+Ba2++2OH-═NH3•H2O+BaSO4↓+H2O |
20.下表是元素周期表中短周期的一部分,则下列说法正确的是( )
| X | ||
| M | Y | |
| Z | N |
| A. | 元素Y与元素Z的最高正化合价之和的数值等于13 | |
| B. | 元素Z的含氧酸的酸性比元素N的强 | |
| C. | 离子半径的大小顺序为Z(n+1)->M(n+1)->Yn- | |
| D. | Z的气态氢化物的还原性和热稳定性均比N强 |
17.下列关于0.3mol氧气和0.2mol臭氧气(O3)的说法正确的是( )
| A. | 原子数之比为3:2 | B. | 同温同压下密度比是2:3 | ||
| C. | 同温同压下质量比是3:2 | D. | 标准状况下体积比是2:3 |
14.如表各组关于强电解质、弱电解质、非电解质的归类正确的( )
| A | B | C | D | |
| 强电解质 | C | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | HCl | H2O |
| 非电解质 | 蔗糖 | BaSO4 | C2H5OH | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
15.在8NH3+3Cl2=N2+6NH4Cl反应中,若有标准状态下3.36LCl2参加反应,则被氧化的NH3的质量为( )
| A. | 13.6g | B. | 10.2g | C. | 6.8g | D. | 1.7g |

 ,
, .写出H→I的反应方程式
.写出H→I的反应方程式 .
. 或
或 .
.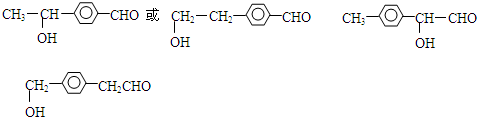 .
.