题目内容
8.下列说法错误的是( )| A. | 在共价化合物中一定含有共价键 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 双原子单质分子中的共价键一定是非极性键 |
分析 A、只含有共价键的化合物是共价化合物;
B、全部由非金属元素组成的化合物可能是离子化合物,离子化合物一定含有离子键;
C、离子化合物一定含有离子键;
D、同种元素形成的纯净物是单质,而同种元素的原子形成的共价键是非极性共价键.
解答 解:A、只含有共价键的化合物是共价化合物,所以在共价化合物中一定含有共价键,故A正确;
B、全部由非金属元素组成的化合物可能是离子化合物,如氯化铵中只含有非金属元素,但氯化铵是离子化合物,故B错误;
C、离子化合物一定含有离子键,所以含有离子键的化合物是离子化合物,故C正确;
D、同种元素形成的纯净物是单质,而同种元素的原子形成的共价键是非极性共价键,故D正确;
故选B.
点评 本题考查了化学键和化合物的关系,难度不大,注意全部由非金属元素组成的化合物可能是离子化合物,由金属元素和非金属元素组成的化合物可能是共价化合物,如氯化铝.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
19.下列各对物质中互为同系物的是( )
| A. | CH3-CH=CH2和CH3-CH2-CH=CH2 | B. | CH3-CH3和CH3-CH=CH2 | ||
| C. | CH3-CH2-CH3和CH3-CH=CH2 | D. | CH3-CH2-CH2-CH3和CH3-CH2-CHCl2 |
3.下列说法正确的是( )
| A. | 沸点由高到低:癸烷、正已烷、新戊烷、正戊烷 | |
| B. | 酸性高锰酸钾溶液既可以鉴别甲烷和乙烯,又可以用来除去甲烷中的少量乙烯 | |
| C. | 乙烯的化学性质比乙烷活泼,可作香蕉等水果的催熟剂 | |
| D. | 苯可以通过石油分馏或煤焦油的催化重整获得 |
13.下表为部分短周期元素化合价及其相应原子半径的数据.请回答下列问题:
(1)元素G在周期中的位置是第二周期ⅣA族;元素F所形成的常见单质的电子式为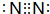 .
.
(2)A、C、E的氢化物稳定性顺序由大到小是HF>H2O>H2S.(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是SOCl2+H2O=SO2↑+2HCl.
(4)请写出B的单质的一种重要用途用作半导体材料、制造合金、光电池、计算机芯片等.
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合价 | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合价 | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
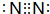 .
.(2)A、C、E的氢化物稳定性顺序由大到小是HF>H2O>H2S.(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是SOCl2+H2O=SO2↑+2HCl.
(4)请写出B的单质的一种重要用途用作半导体材料、制造合金、光电池、计算机芯片等.

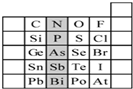 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.请用元素符号或化学式填空:
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.请用元素符号或化学式填空: ,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为
,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为 .
.