题目内容
6.下列化合物中,在常温常压下以液态形式存在的是( )| A. | 丙三醇 | B. | 乙炔 | C. | 丙烯 | D. | 丁烷 |
分析 常见有机物中常温下为气态有:C原子数≤4烃、新戊烷、一氯甲烷、甲醛等,据此判断.
解答 解:A.丙三醇是液体,故A正确;
B.乙炔是气体,故B错误;
C.丙烯是气体,故C错误;
D.丁烷是气体,故D错误.
故选A.
点评 本题考查烃类的物理性质,难度不大,注意知识的积累.

练习册系列答案
相关题目
16.下列溶液中NO3-的物质的量浓度最大的是( )
| A. | 500 mL 1 mol•L-1的KNO3溶液 | |
| B. | 500 mL 1 mol•L-1的Ba(NO3)2溶液 | |
| C. | 1000 mL 0.5 mol•L-1的Mg(NO3)2溶液 | |
| D. | 1000 mL 0.5 mol•L-1的Fe(NO3)3溶液 |
14. (1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
(1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
复分解反应存在这样一个规律:一种较强酸(或碱性较强的物质)可以自发地反应生成较弱酸(或碱性较弱的物质).照该规律,请判断下列反应不能成立的是CD (填编号).
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前述信息判断,浓度均为0.05mol•L-1的下列六种物质的溶液中,pH最小的是⑤ (填编号);将各溶液分别稀释100倍,pH变化最小的是① (填编号).
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-.
(4)标准状况下,向1L含NaOH、Ca(OH)2各0.1mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图.
 (1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
(1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:| 溶质 | CH3CO ONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前述信息判断,浓度均为0.05mol•L-1的下列六种物质的溶液中,pH最小的是⑤ (填编号);将各溶液分别稀释100倍,pH变化最小的是① (填编号).
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-.
(4)标准状况下,向1L含NaOH、Ca(OH)2各0.1mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图.
1.下列化学用语正确的是( )
| A. | 聚丙烯的结构简式为: | B. | 丙烷分子的球棍模型为: | ||
| C. | 四氯化碳分子的电子式为: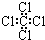 | D. |  的分子式是:C6H12O 的分子式是:C6H12O |
11.以下能级符号不正确的是( )
| A. | 3s | B. | 3p | C. | 3d | D. | 2d |
18.下列说法中正确的是( )
| A. | 二次电池在充电时,电池的负极要与外接电源的负极相连 | |
| B. | 用惰性电极电解硫酸铜溶液一段时间后,加入氢氧化铜可恢复原状 | |
| C. | 化学腐蚀是生活中最常见的一种金属腐蚀 | |
| D. | 燃料电池中的电极材料必须活性不同 |
15.在密闭容器中进行反应:A(g)+2B(g)?3C(g)+D(s),有关下列图象的说法不正确的是( )
| A. |  依据图可判断正反应为放热反应 | |
| B. |  在图中,虚线可表示压缩反应装置体积的情况 | |
| C. |  若正反应的△H>0,图可表示升高温度使平衡向逆反应方向移动 | |
| D. |  由图中混合气体的平均相对分子质量随温度的变化情况,可推知逆反应的△H<0 |
7.下列各有机化合物的命名正确的是( )
| A. | CH2═CH-CH═CH2 1,3二丁烯 | B. |  3丁醇 3丁醇 | ||
| C. |  甲基苯酚 甲基苯酚 | D. |  2甲基丁烷 2甲基丁烷 |
 化学在能源开发与利用中起着十分重要的作用.
化学在能源开发与利用中起着十分重要的作用.