题目内容
4.为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:【探究一】
(1)常温下,工业上用铁质容器盛放冷的浓硫酸,其原因是常温下,铁遇浓硫酸发生钝化现象.
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y.
①甲同学认为X中除Fe3+之外还可能含有Fe2+.若要确认其中的Fe2+,应选用d(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此可求算气体Y中SO2的体积分数.
写出探究②中出现的所有离子反应方程式SO2+Br2+2H2O=SO42-+2Br-+4H+、SO42-+Ba2+=BaSO4↓.
【探究二】
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g•L-1.为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应).
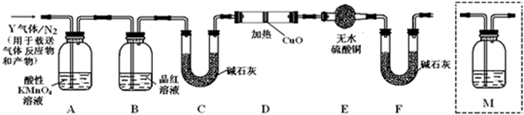
(3)装置B中试剂的作用是检验SO2是否除尽.
(4)分析Y气体中的Q2气体是如何生成的C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.(用化学方程式表示).
(5)为确认Q2的存在,需在装置中添加洗气瓶M于c(选填序号).
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是D中固体由黑色变红色和E中固体由白色变蓝色.
分析 (1)常温下,铁遇冷的浓硫酸发生钝化现象;
(2)①亚铁离子有还原性,能还原酸性高锰酸钾溶液而使其褪色;
②根据硫酸钡与二氧化硫的关系式计算二氧化硫的体积,再根据体积分数公式计算;
(3)二氧化硫能使品红溶液褪色,据此判断是否含有二氧化硫;
(4)碳素钢中含有碳,加热条件下,碳和浓硫酸反应生成二氧化碳;
(5)用澄清石灰水检验二氧化碳,首先要排除二氧化硫的干扰;
(6)M是密度最小的气体,所以M是氢气,氢气具有还原性,能含有氧化铜同时生成水,水能使无水硫酸铜变蓝.
解答 解:(1)常温下,铁遇冷的浓硫酸发生氧化还原反应,在铁表面生成一层致密的氧化物薄膜而阻止了进一步的反应,即发生钝化现象,所以反应片刻后取出观察,铁钉表面无明显变化,
故答案为:常温下,铁遇浓硫酸发生钝化现象;
(2)①亚铁离子具有还原性,而酸性高锰酸钾有氧化性,发生氧化还原反应使高锰酸钾溶液褪色,铁离子和亚铁离子同时存在时,应该用酸性高锰酸钾溶液检验亚铁离子,故d正确,
故答案为:d;
②气体Y中含有二氧化硫,可能含有二氧化碳等其他气体,二氧化碳不与氯化钡溶液反应,所以二氧化硫与溴水发生氧化反应生成硫酸根离子,硫酸根离子与比利时反应生成硫酸钡白色沉淀,离子方程式是SO2+Br2+2 H2O=SO42-+2Br-+4H+、SO42-+Ba 2+=BaSO4↓,
故答案为:SO2+Br2+2 H2O=SO42-+2Br-+4H+、SO42-+Ba 2+=BaSO4↓;
(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽,
故答案为:检验SO2是否除尽;
(4)碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(5)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,即在通入碱石灰之前检验,
故答案为:c;
(6)M是密度最小的气体,所以M是氢气,氢气具有还原性,能还原黑色的氧化铜生成红色的铜单质,同时生成水,水能使无水硫酸铜变蓝色,这是检验水的特征反应,所以如果D中氧化铜变红,E中无水硫酸铜变蓝,则证明含有氢气,
故答案为:D中固体由黑色变红色和E中固体由白色变蓝色.
点评 本题考查性质实验方案的设计与评价,题目难度中等,涉及浓硫酸的性质、二氧化硫的性质、常见物质的检验等知识点,侧重于考查学生综合运用化学知识的能力和实验能力,注意常温下铁和冷的浓硫酸不是不反应,而是反应生成了致密的氧化物薄膜而阻止了进一步反应,为易错点.

| A. | 硫酸溶液与氢氧化钡溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| B. | 氯化钙溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| C. | 硫酸铜溶液中加入烧碱溶液:Cu2++2OH-═Cu(OH)2↓ | |
| D. | 碳酸钙固体上滴加醋酸溶液:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
 学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:
学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:(1)下列是某同学对有关物质进行分类的列表:
| | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | SO2 |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
(2)下列2个反应,按要求填写相关量.
①2Na2O2+2H2O=4NaOH+O2反应中,每消耗lmol Na2O2生成16g O2;
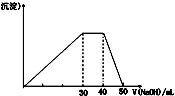
②除去NaCl溶液中少量的Na2SO4.杂质,要判断所加BaCl2溶液是否过量,可向滤液中加入X溶液.X可以是D填代号)
A.NaOH B.AgNO3 C.HCI D.Na2SO4
(3)配平下面化学方程式,回答下列问题:
3C+2K2Cr2O7+8H2SO4=2K2SO4+CO2↑+Cr2(SO4)3+8H2O
①H2SO4在上述反应中表现出来的性质是(填选项编号)C.
A.氧化性. B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为4.48L.
| A. | 过氧化钠可用作漂白剂和呼吸面具中的供氧剂 | |
| B. | 钠和钾的合金常温下是固体,可用于快中子反应堆作热交换剂 | |
| C. | 碳酸氢钠是焙制糕点所用的发酵粉之一,也可以用于治疗胃酸过多 | |
| D. | 热的碳酸钠溶液可以去除物品表面的油污 |
| A配置0.10mol/LNaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中的I2分出水层后的操作 | D.记录滴定终点读数为12.20mL |
 |  |  |  |
| A. | 配制0.10mol/L NaOH溶液 | |
| B. | 除去CO中的CO2 | |
| C. | 苯萃取碘水中的I2分出水层后的操作 | |
| D. | 记录滴定终点读数为12.20mL |
| A. | Fe跟FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | Fe跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | FeCl3与Cl2反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3跟硝酸反应:Fe(OH)3+3H+═Fe3++3H2O |
 .
.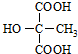 (或
(或 ).
).