题目内容
元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法合理的是( )
| A、若X、Y都是气态氢化物,且相对分子质量:X>Y,则沸点:X>Y |
| B、若R2-和M+的电子层结构相同,则原子序数:R>M |
| C、若X、Y属于同主族元素,且相对原子质量:X>Y,则X失电子能力比Y强 |
| D、若M、N是同主族元素,且原子序数:M>N,则非金属性:M>N |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.元素气态氢化物的沸点一般随相对分子质量增大而增大,但含有氢键的物质的沸点较高;
B.电子层结构相同的阴阳离子,阳离子的原子序数大于阴离子;
C.同主族自上而下金属性增强;
D.同一主族元素,元素的非金属性随着原子序数的增大而减小;
B.电子层结构相同的阴阳离子,阳离子的原子序数大于阴离子;
C.同主族自上而下金属性增强;
D.同一主族元素,元素的非金属性随着原子序数的增大而减小;
解答:
解:A.元素气态氢化物的沸点一般随相对分子质量增大而增大,但含有氢键的物质的沸点较高,如水的沸点高于硫化氢,故A错误;
B.电子层结构相同的阴阳离子,阳离子的原子序数大于阴离子,所以R<M,故B错误;
C.X、Y属于同主族元素,且相对原子质量:X>Y,同主族自上而下金属性增强,故X失电子能力比Y强,故C正确;
D.若M、N是同主族元素,且原子序数:M>N,则非金属性:M<N,故D错误;
故选C.
B.电子层结构相同的阴阳离子,阳离子的原子序数大于阴离子,所以R<M,故B错误;
C.X、Y属于同主族元素,且相对原子质量:X>Y,同主族自上而下金属性增强,故X失电子能力比Y强,故C正确;
D.若M、N是同主族元素,且原子序数:M>N,则非金属性:M<N,故D错误;
故选C.
点评:本题考查元素周期表结构、元素周期律等知识,题目难度不大,注意对规律的理解掌握,注意A选项中氢键存在.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.30×10-5mol/L.若在5mL含有KCl和KI浓度均为0.01mol/L的混合溶液中,滴加8mL 0.01mol/L的AgNO3溶液,则下列叙述中不正确的是A( )
| A、反应后溶液中离子浓度大小关系为:c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B、发生反应生成的AgI沉淀多于AgCl沉淀 |
| C、在水中AgCl的溶解度比AgI的溶解度大 |
| D、若在AgCl悬浊液中滴加KI溶液,白色沉淀会转变成黄色沉淀 |
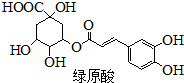 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )| A、奎尼酸分子式为C7H14O6 |
| B、绿原酸能发生取代、加成、消去和缩聚反应 |
| C、1mol奎尼酸与NaOH溶液反应,最多消耗5molNaOH |
| D、咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应 |
下列化合物中所有原子或离子都满足最外层8电子或2电子结构的是( )
| A、乙硼烷B2H6 |
| B、氢化钠NaH |
| C、六氟化氙XeF6 |
| D、四氯化碳CCl4 |
化学式为C16H23Cl3O2的有机物分子内不含有碳碳叁键,它所含的双键数目最多是( )
| A、5 | B、4 | C、3 | D、2 |
阿伏加德罗常数为NA,下列说法错误的是( )
| A、16gO2中含有的氧气分子数为0.5NA |
| B、常温常压下,1molNe含有的原子数为NA |
| C、1.6gCH4中含有的甲烷分子数为0.1NA |
| D、1mol/LNaCl溶液中含有的钠离子数为NA |
 有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.
有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.