题目内容
下列化合物中所有原子或离子都满足最外层8电子或2电子结构的是( )
| A、乙硼烷B2H6 |
| B、氢化钠NaH |
| C、六氟化氙XeF6 |
| D、四氯化碳CCl4 |
考点:原子核外电子排布
专题:
分析:分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断,离子化合物根据得失电子来判断.
解答:
解:A、B2H6中,B原子的原子核外最外层电子数为3,其在分子中的化合价为-3价,在分子中的原子最外层电子数为6,故A错误;
B、NaH为离子化合物,Na原子的原子核外最外层电子数为1,失去一个电子达8电子稳定结构,氢原子最外层一个电子,得一个电子达到2电子稳定结构,故B正确;
C、六氟化氙中,氙原子的原子核外最外层电子数为8,其在分子中的化合价为+6价,在分子中的原子最外层电子数为14,故C错误;
D、CCl4中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,在分子中的原子最外层电子数为8,Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,在分子中的原子最外层电子数为8,故D正确;
故选BD.
B、NaH为离子化合物,Na原子的原子核外最外层电子数为1,失去一个电子达8电子稳定结构,氢原子最外层一个电子,得一个电子达到2电子稳定结构,故B正确;
C、六氟化氙中,氙原子的原子核外最外层电子数为8,其在分子中的化合价为+6价,在分子中的原子最外层电子数为14,故C错误;
D、CCl4中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,在分子中的原子最外层电子数为8,Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,在分子中的原子最外层电子数为8,故D正确;
故选BD.
点评:本题考查原子的结构,本题中注意判断是否满足8电子或2电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子或2电子结构是解答的关键.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
满足通式CnH2nO的有机物甲,既可被氧化为一元羧酸乙,又可被还原为一元醇丙,乙和丙在一定条件下反应生成酯丁,则下列说法正确的是( )
| A、甲和丁的最简式相同 |
| B、丁的分子量是丙的两倍 |
| C、甲既可是饱和一元醛,又可是饱和一元酮 |
| D、甲的分子中一定具有甲基 |
对实验I-IV的实验现象预测错误的是( )
A、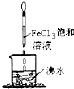 继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
B、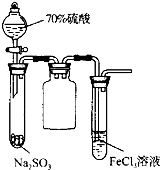 实验试管中出现淡黄色浑浊 |
C、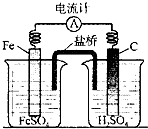 实验中碳棒上有无色气泡产生 |
D、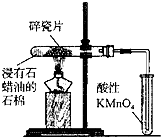 实验中酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法合理的是( )
| A、若X、Y都是气态氢化物,且相对分子质量:X>Y,则沸点:X>Y |
| B、若R2-和M+的电子层结构相同,则原子序数:R>M |
| C、若X、Y属于同主族元素,且相对原子质量:X>Y,则X失电子能力比Y强 |
| D、若M、N是同主族元素,且原子序数:M>N,则非金属性:M>N |
下列实验操作中正确的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏操作时,应使温度计水银球插入液面以下 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,0.1NA个水分子所占的体积大于2.24L |
| B、标准状况下,22.4LCCl4含有的原子数为4NA |
| C、标准状况下,14gN2含有的核外电子数为7NA |
| D、3molFe与足量的盐酸充分反应,转移9NA个电子 |


 A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:
A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空: