��Ŀ����
7����Na2SO3��Һ�Ͳ�ͬ��������������Һ��Ϊʵ�����̽���ε����ʺ�����Һ�䷴Ӧ�Ķ����ԣ�| ʵ�� | �Լ� | ���� | |
| �ι� | �Թ� | ||
 | 0.2 mol•L-1 Na2SO3��Һ | ����Ag2SO4��Һ | ������ɫ���� |
| 0.2 mol•L-1 CuSO4 | ����Һ���̣������μӲ����ػ�ɫ���� | ||
| 0.1 mol•L-1 Al2��SO4��3��Һ | ��ʼ�����Ա仯�������μӲ�����ɫ���� | ||
��2�������飬�������ػ�ɫ�����в���SO42-������Cu+��Cu2+��SO32-��
��֪��Cu+$\stackrel{ϡ����}{��}$Cu+Cu2+��Cu2+$\stackrel{I-}{��}$CuI������ɫ��+I2��
����ϡ����֤ʵ�����к���Cu+��ʵ��������������ɫ���壮
��ͨ������ʵ��֤ʵ�������к���Cu2+��SO32-��

a����ɫ����A��BaSO4���Լ�1��HCl��BaCl2��Һ��
b��֤ʵ�����к���Cu2+��SO32-����������I-�������£�Cu2+ת��Ϊ��ɫ����CuI��SO32-ת��ΪSO42-��
��3����֪��Al2��SO3��3��ˮ��Һ�в����ڣ������飬�����İ�ɫ��������SO42-���ð�ɫ������������ǿ�ᣬ��������ǿ�����ʹ����KMnO4��Һ��ɫ��
���Ʋ�����к������������Al��OH��3��
�ڶ��ڳ�������������Ĵ�����ʽ������ּ��裺i����Al��OH��3��������ii�����������ļ�ʽ���У��Լ���ii����˶Ա�ʵ�飬֤ʵ�˼���ii������
a�����Ա�ʵ�鷽������������
����һ��
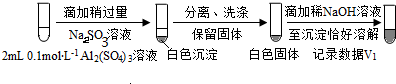
�������
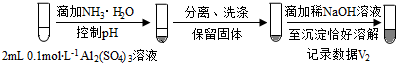 ����ͼ��ʽ���֣���
����ͼ��ʽ���֣���b������ii������ʵ��֤����V1���Դ���V2
��4������ʵ�飬�������ε��������ܽ��ԡ���ԭ�ԡ���ˮ��Һ�гʼ��ԣ�����Һ�䷴Ӧ�Ķ���������������Һ�����������ӵ����ʺͷ�Ӧ�����йأ�
���� ��1��0.2mol/LNa2SO3��Һ���뱥��Ag2SO4��Һ������Ӧ���ɰ�ɫ����Ag2SO3��
��2���ٸ��ݵڶ���������2����֪��Ϣ�����Ե�֪��ȡ����ϴ�����ų�Cu2+���ţ����ػ�ɫ�������μ�ϡ���ᣬ������죨ͭ���ʣ�����֤���� Cu+��
��a������BaSO4������֪��������Լ�Ϊ��Ba2+�Ļ��������ѡ��BaCl2��
b���ɰ�ɫ����A��֪֮ǰ��ȡ�ϲ���Һ����SO42-���ɼ���KI���ɰ�ɫ������֪�ػ�ɫ�����к���Cu2+��Cu2+��I-��������CuI��ɫ�������ɼӵ���������˵���ϲ���Һ����I2����Cu2+��I-��Ӧ����I2������ƶ����ɵ�I2������������Ӧ������л�ԭ��SO32-��
��3���������⣬��ɫ������������ǿ�ᣬ��������ǿ����Եõ������к���Al3+��OH-����ʹ����KMnO4��Һ��ɫ����Ϊ�����л�ԭ�Ե�����������ӣ�
�ڸ���ʵ��Ŀ�ĺͶԱ�ʵ�����ԭ�����н��
��4������ʵ�飬�������ξ����ܽ��ԡ���ԭ�ԡ�ˮ��ʼ��ԣ�����Һ�䷴Ӧ�Ķ���������������Һ�����������ӵ����ʺͷ�Ӧ�����йأ�
��� �⣺��1��ʵ�����0.2mol/LNa2SO3��Һ���뱥��Ag2SO4��Һ������Ag2SO4������Һ����Һ��Ϻ�ϡ�ͣ���˲�������Ag2SO4����������SO32-Ũ�Ƚϴ�����ƶϰ�ɫ����ΪAg2SO3����Ӧ�����ӷ���ʽΪ��2Ag++SO32-=Ag2SO3�����ʴ�Ϊ��2Ag++SO32-=Ag2SO3����
��2�������ݷ�ӦCu+��ϡ���ᷴӦͭ��ͭ���ӣ��������к���Cu+������ϡ����ᷢ���绯��Ӧ����ͭ���ʣ�ʵ���������к�ɫ�������ɣ�
�ʴ�Ϊ��������ɫ���壻
��a������ʵ�����̿�֪ʵ��ԭ��Ϊ2Cu2++4I-=2CuI+I2��I2+SO32-+H2O=SO42-+2I-+2H+��SO42-+Ba2+=BaSO4��������BaSO4������֪��������Լ�Ϊ��Ba2+�Ļ��������ѡ��BaCl2��Һ�����dz���Aû��BaSO3�����Ӧ�����Ի����У�
�ʴ�Ϊ��HCl��BaCl2��Һ��
b���ɰ�ɫ����A��֪֮ǰ��ȡ�ϲ���Һ����SO42-���ɼ���KI���ɰ�ɫ������֪�ػ�ɫ�����к���Cu2+��Cu2+��I-��������CuI��ɫ�������ɼӵ���������˵���ϲ���Һ����I2����Cu2+��I-��Ӧ����I2������ƶ����ɵ�I2������������Ӧ������л�ԭ��SO32-��
�ʴ�Ϊ���ػ�ɫ������KI��Һ��Ӧ���ɰ�ɫ������CuI����֤������Cu2+����ɫ����AΪ���ᱵ��֤������SO32-��
��3���ٸ�������֪ʵ���İ�ɫ��������SO42-���ð�ɫ������������ǿ�ᣬ��������ǿ�����ʹ����KMnO4��Һ��ɫ�������Ʋ�����к���Al3+��OH-����ʹ����KMnO4��Һ��ɫ����Ϊ�����л�ԭ�Ե�����������ӣ�
�ʴ�Ϊ��Al3+��OH-��
�ڸ��ݼ����֪ʵ���Ŀ����֤�������ij�����Al��OH��3�������ļ�ʽ�Σ�����ʵ�������Ʊ���������еij�����Ȼ����õμ�NaOH��Һ����˶Ա�ʵ������Ҫ�Ʊ���Al��OH��3������Ȼ��μ�NaOH��Һ�����������ĵ�NaOH�����ͬ����������еij�������Al��OH��3���������������ĵ�NaOH�����ͬ����������еij������������ļ�ʽ�Σ�
���ļ�ʽ�κ�NaOH��Һ��Ӧ�൱�������Ӻ�NaOH��Ӧ����Ӧ����Ϊ1��4����Al��OH��3��NaOH��Ӧ����Ϊ1��1�������V1���Դ���V2�������ii��������V1=V2�������i������
�ʴ�Ϊ��a�� ��
��
b������ii������ʵ��֤����V1���Դ���V2��
�ʴ�Ϊ��V1���Դ���V2��
��4����Ŀ���жദ��ʾ���ǻ�ԭ�ԣ����磨3���еij�������ʹ���Ը��������ɫ���ڶ��գ�ʵ�����Ҫ����ʵ��Ŀ�ģ�������Ŀ������̽������ Na2SO3��Һ�Ͳ�ͬ��������������Һ��Ӧ�����Եõ����ۣ�����Һ�䷴Ӧ�Ķ���������������Һ�����������ӵ����ʺͷ�Ӧ�����йأ�
�ʴ�Ϊ����ԭ�ԡ�ˮ��ʼ��ԣ���������Һ�����������ӵ����ʺͷ�Ӧ�����йأ�
���� ���⿼�黯ѧʵ�鷽���ķ��������ۺ���ƣ���Ҫ�����Ӽ����ʵ����̵�����Ӧ�ã���Ŀ�ѶȽϴ�

| A�� | H+��OH-��NO3- | B�� | Ba2+��H+��SO42- | C�� | K+��OH-��CO32- | D�� | Fe3+��Cl-��OH- |
| A�� | ����0.1molNH3•H2O | |
| B�� | ��Һ��NH3�����ʵ���Ũ��Ϊ0.2mol•L-1 | |
| C�� | NH3��NH3•H2O�����ʵ���Ũ��֮��Ϊ0.2mol•L-1 | |
| D�� | NH3��NH3•H2O��NH4+�����ʵ���֮��Ϊ0.1mol |
| A | B | C | D |
| ����ũ���ݾ������أ�����ܡ�ֹ���������� | ̼������ҩƬ |  |  |
| �Ŵ��й�������������ƿ��� | ��ҩ�ǿ���ҩ������ʱ��Щ�������ҩЧ | �����иñ�־�Ķ����ӦԶ�벢���� | ���иñ�־����Ʒ�ǿɻ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | c��Na+����c��CH3COO-����c��H+����c��OH-�� | B�� | c��Na+����c��CH3COO-����c��OH-����c��H+�� | ||
| C�� | c��OH-����c��H+����c��Na+����c��CH3COO-�� | D�� | c��Na+��=c��CH3COO-����c��OH-����c��H+�� |
| A�� | 3.5 mol/L | B�� | 4.5 mol/L | C�� | 7.0 mol/L | D�� | 9.0 mol/L |
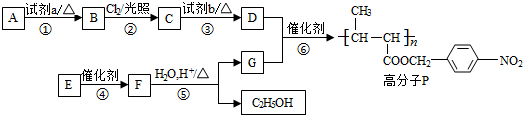
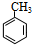 ��
��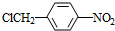 +NaOH$��_{��}^{ˮ}$
+NaOH$��_{��}^{ˮ}$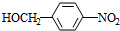 +NaCl��
+NaCl��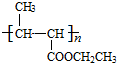 +nH2O$��_{��}^{H+}$
+nH2O$��_{��}^{H+}$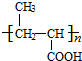 +n CH3CH2OH��
+n CH3CH2OH��
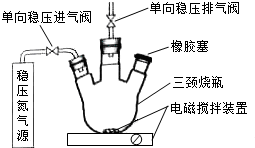 ˮ����������DO���Ǻ���ˮ���Ծ�������һ��ָ�꣬ͨ����ÿ��ˮ���ܽ������ӵ�������ʾ����λmg•L-1���ҹ����ر�ˮ�������������涨����������ˮԴ��DO���ܵ���5mg•L-1��ij��ѧС��ͬѧ���������װ�ã��г�װ���ԣ����ⶨij��ˮ��DO��
ˮ����������DO���Ǻ���ˮ���Ծ�������һ��ָ�꣬ͨ����ÿ��ˮ���ܽ������ӵ�������ʾ����λmg•L-1���ҹ����ر�ˮ�������������涨����������ˮԴ��DO���ܵ���5mg•L-1��ij��ѧС��ͬѧ���������װ�ã��г�װ���ԣ����ⶨij��ˮ��DO��