题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、常温下,1L0.1mol/L的BaCl2溶液中Cl-数为0.2NA |
| B、1mol羟基中电子数为10NA |
| C、17.6g丙烷中所含的极性共价键为4NA个 |
| D、常温常压下,22.4L乙烯中C-H键数为4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1L0.1mol/L的BaCl2溶液中含有0.1mol氯化钡,含有0.2mol氯离子;
B.羟基中含有9个电子,1mol羟基中含有9mol电子;
C.丙烷分子中存在的极性共价键为碳氢键,丙烷分子中含有8个碳氢极性键;
D.常温常压下,不是标况下,不能使用标况下的气体摩尔体积计算乙烯的物质的量.
B.羟基中含有9个电子,1mol羟基中含有9mol电子;
C.丙烷分子中存在的极性共价键为碳氢键,丙烷分子中含有8个碳氢极性键;
D.常温常压下,不是标况下,不能使用标况下的气体摩尔体积计算乙烯的物质的量.
解答:
解:A.1L0.1mol/L的BaCl2溶液中含有0.1mol氯化钡,0.1mol氯化钡中含有0.2mol氯离子,含有的氯离子数为0.2NA,故A正确;
B.1mol羟基中含有9mol电子,含有的电子数为9NA,故B错误;
C.17.6g丙烷的物质的量为:
=0.4mol,0.4mol丙烷分子中含有的极性键的物质的量为:0.4mol×8=3.2mol,所含的极性共价键为3.2NA,故C错误;
D.不是标况下,不能使用标况下的气体摩尔体积计算22.4L乙烯的物质的量,故D错误;
故选A.
B.1mol羟基中含有9mol电子,含有的电子数为9NA,故B错误;
C.17.6g丙烷的物质的量为:
| 17.6g |
| 44g/mol |
D.不是标况下,不能使用标况下的气体摩尔体积计算22.4L乙烯的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,选项B为易错点,注意羟基与氢氧根离子、甲烷与甲基的区别.

练习册系列答案
相关题目
下列烧杯中盛放的都是稀H2SO4,在Cu电极上产生大量气泡的是( )
A、 |
B、 |
C、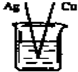 |
D、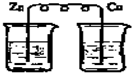 |
下列离子方程式正确的是( )
| A、氢氧化镁中滴加盐酸:H++OH-═H2O |
| B、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、已知电离平衡常数:H2CO3>HClO>HCO3-,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- |
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
下列表述正确的是( )
A、H2O2的电子式: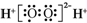 | ||
B、Cl的原子结构示意图: | ||
C、质子数是82,中子数是122的铅原子:
| ||
D、CO2的比例模型: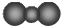 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2molNa被完全氧化生成1mol Na2O2,得到2NA个电子 |
| B、在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 |
下列关于胶体的说法中正确的是( )
| A、胶体外观不均匀 |
| B、胶体不能通过滤纸 |
| C、胶体粒子不停地无秩序运动 |
| D、胶体不稳定,静止后容易形成沉淀 |
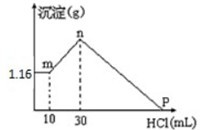 把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示:
把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示: