题目内容
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A、达到化学平衡时,4υ正(O2)=5υ逆(NO) |
| B、若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C、达到化学平衡时,若增加容器体积,则正反应速率增大,逆反应速率减少 |
| D、化学反应速率关系是:2υ正(NH3)=3υ正(H2O) |
考点:化学反应速率和化学计量数的关系,化学平衡状态的判断
专题:
分析:A.不同物质的正逆反应速率之比等于化学计量数之比,达到平衡状态;
B.生成x mol NO的同时,消耗x mol NH3,均体现正反应速率关系;
C.增加容器体积,压强减小;
D.化学反应速率之比等于化学计量数之比.
B.生成x mol NO的同时,消耗x mol NH3,均体现正反应速率关系;
C.增加容器体积,压强减小;
D.化学反应速率之比等于化学计量数之比.
解答:
解:A.不同物质的正逆反应速率之比等于化学计量数之比,达到平衡状态,则达到化学平衡时,4υ正(O2)=5υ逆(NO),故A正确;
B.生成x mol NO的同时,消耗x mol NH3,均体现正反应速率关系,不能判断平衡状态,故B错误;
C.增加容器体积,压强减小,则正、逆反应速率均减小,故C错误;
D.化学反应速率之比等于化学计量数之比,则化学反应速率关系是:3υ正(NH3)=2υ正(H2O),故D错误;
故选A.
B.生成x mol NO的同时,消耗x mol NH3,均体现正反应速率关系,不能判断平衡状态,故B错误;
C.增加容器体积,压强减小,则正、逆反应速率均减小,故C错误;
D.化学反应速率之比等于化学计量数之比,则化学反应速率关系是:3υ正(NH3)=2υ正(H2O),故D错误;
故选A.
点评:本题考查化学反应速率及化学计量数的关系,为高频考点,涉及平衡状态判断、影响反应速率的因素等,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
已知PH=5的MgCl2溶液中含有杂质FeCl3,为除去杂质可加入的试剂是( )
| A、MgO |
| B、Mg(NO3)2 |
| C、NaOH |
| D、NaHCO3 |
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成①肯定不含I-②肯定不含Cu2+③肯定含SO32-④可能含I-⑤可能含SO32-的判断正确的是( )
| A、①②③ | B、②④⑤ |
| C、①②⑤ | D、②③④ |
常温下,一定浓度的某溶液,由水电离出的c(OH--)=10--4mol/L,则该溶液中的溶质可能是( )
| A、Na2SO4 |
| B、CH3COOH |
| C、NaOH |
| D、CH3COOK |
对溶液中的离子反应有下列说法中正确的是( )
①不可能是氧化还原反应;②只能是复分解反应;③有可能是置换反应;④不可能有分子参加.
①不可能是氧化还原反应;②只能是复分解反应;③有可能是置换反应;④不可能有分子参加.
| A、①② | B、只有③ | C、②④ | D、①④ |

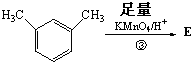 其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为
其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为