题目内容
下列说法错误的是( )
| A、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| B、硅酸盐NaAISiO4.nH2O可改写成氧化物形式为:Na2O.AI2O3.2SiO2.2nH2O |
| C、AI65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属Al、Cu、Fe都大 |
| D、过量铁与浓硫酸加热反应可以得到氢气 |
考点:二氧化硫的污染及治理,浓硫酸的性质,含硅矿物及材料的应用,铁的化学性质
专题:
分析:A、正常的雨水溶解二氧化碳,其pH为5.6,pH值小于5.6为酸雨,pH由4.68变为4.28,主要是雨水中溶解的二氧化硫生成亚硫酸,亚硫酸被氧化为硫酸;
B、硅酸盐NaAlSiO4.nH2O可改写成氧化物形式为:Na2O.Al2O3.2SiO2?2nH2O
C、合金的硬度一般比各成分金属大;
D、因为随着反应的进行,浓硫酸会稀释成稀硫酸,所以可以生成氢气.
B、硅酸盐NaAlSiO4.nH2O可改写成氧化物形式为:Na2O.Al2O3.2SiO2?2nH2O
C、合金的硬度一般比各成分金属大;
D、因为随着反应的进行,浓硫酸会稀释成稀硫酸,所以可以生成氢气.
解答:
解:A、正常的雨水溶解二氧化碳,其PH为5.6,pH值小于5.6为酸雨,pH由4.68变为4.28,主要是雨水中溶解的二氧化硫生成亚硫酸,亚硫酸被氧化为硫酸,由弱酸转化为强酸,酸性增强,故A错误;
B、硅酸盐NaAlSiO4.nH2O可改写成氧化物形式为:Na2O.Al2O3.2SiO2?2nH2O,故B正确;
C、拟晶具有合金的某些优良物理性能,合金的硬度一般比各成分金属大,故C正确;
D、因为随着反应的进行,浓硫酸会稀释成稀硫酸,所以可以生成氢气,故D正确.
故选A.
B、硅酸盐NaAlSiO4.nH2O可改写成氧化物形式为:Na2O.Al2O3.2SiO2?2nH2O,故B正确;
C、拟晶具有合金的某些优良物理性能,合金的硬度一般比各成分金属大,故C正确;
D、因为随着反应的进行,浓硫酸会稀释成稀硫酸,所以可以生成氢气,故D正确.
故选A.
点评:本题考查化学与生产、生活相关的知识,比较基础,是高考考查的热点之一,但涉及知识点较多,灵活运用所学知识进行解答.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
只用水就能鉴别的一组物质是( )
| A、苯酚、乙醇、甘油 |
| B、乙醇、己烯、苯磺酸 |
| C、乙醛、乙二醇、硝基苯 |
| D、苯、乙醇、四氯化碳 |
将一小块钠放入下列溶液中,既能产生气体又能生成白色沉淀的是( )
| A、硝酸铜溶液 | B、稀硫酸 |
| C、氯化钠溶液 | D、氯化镁溶液 |
 已知25℃时,几种难溶电解质的溶度积如下表所示:
已知25℃时,几种难溶电解质的溶度积如下表所示:| 化学式 | AgCl | Ag2S | AgOH |
| 溶度积(K甲 ) | 1.8×10-10 | 6.3×10-50 | 1.5×10-8 |
A、
| ||
B、
| ||
C、
| ||
D、
|
在体积相同的A、B两个带活塞的玻璃容器中,分别注入
体积颜色相同的NO2与溴蒸气,然后将活塞同时向外拉出到
(快速),过一会可以看到( )
| 1 |
| 4 |
| 1 |
| 2 |
| A、A中的颜色比B中的浅 |
| B、A中的颜色比B中的深 |
| C、A中的颜色与B中的深浅相同 |
| D、A中颜色比开始时深 |
关于下列各装置图的叙述不正确的是( )


| A、用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 |
| B、图②装置的盐桥中KCl的Cl-移向甲烧杯 |
| C、图③装置中钢闸门应与外接电源的负极相连获得保护 |
| D、装置④中Ag电极发生反应:2H2O+2e-=H2↑+2OH- |
 ③
③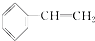 ④
④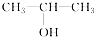 ⑤
⑤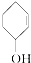 ⑥
⑥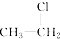
 ⑧
⑧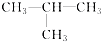 ⑨
⑨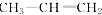 ⑩
⑩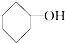 ?
? ?CH3Cl
?CH3Cl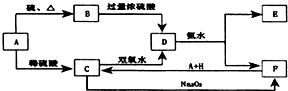 中学化学中几种常见物质的转化关系如图所示:
中学化学中几种常见物质的转化关系如图所示: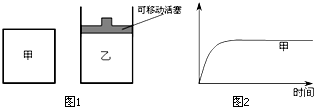 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2?2NH3△H<0.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2?2NH3△H<0.