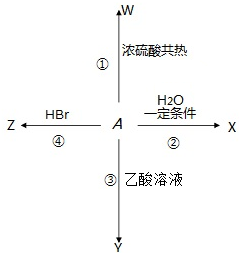
题目内容
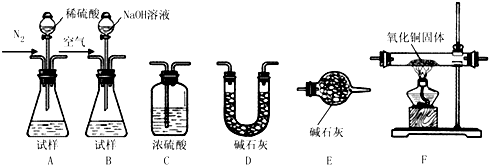
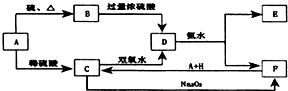 中学化学中几种常见物质的转化关系如图所示:
中学化学中几种常见物质的转化关系如图所示:将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围是
(2)A、B、H的化学式是:
A
(3)①H2O2分子的电子式是
②写出C的酸性溶液与双氧水反应的离子方程式:
(4)写出鉴定D中金属阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程
考点:无机物的推断
专题:推断题
分析:将D溶液滴入沸水中可得到以F为分散质的红褐色液体,说明F为Fe(OH)3;证明D为硫酸铁,E为硫酸铵;由转化关系可知,C为硫酸亚铁,转化关系中A和硫酸反应和硫单质加热反应,说明A为金属单质,转化关系中F(Fe(OH)3)+H+A(Fe)=C(FeSO4),推断A为Fe,B为FeS,H为硫酸,C为硫酸亚铁,被过氧化钠氧化为D硫酸铁,据此答题.
解答:
解:将D溶液滴入沸水中可得到以F为分散质的红褐色液体,说明F为Fe(OH)3;证明D为硫酸铁,E为硫酸铵;由转化关系可知,C为硫酸亚铁,转化关系中A和硫酸反应和硫单质加热反应,说明A为金属单质,转化关系中F(Fe(OH)3)+H+A(Fe)=C(FeSO4),推断A为Fe,B为FeS,H为硫酸,C为硫酸亚铁,被过氧化钠氧化为D硫酸铁,综上所述各物质为:A、Fe;B、FeS;C、FeSO4;D、Fe2(SO4)3;E、(NH4)2SO4;F、Fe(OH)3;H、H2SO4;
(1)红褐色液体是氢氧化铁胶体,分散质粒子直径大小的范围是1nm-100nm,
故答案为:1nm-100nm;
(2)依据推断可知A为Fe,B的化学式为:FeS,H为H2SO4(稀);
故答案为:Fe,FeS,H2SO4(稀);
(3)①因为H2O2是共价化合物,所以分子的电子式为: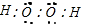 ;
;
故答案为: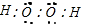 ;
;
②C的酸性溶液与双氧水反应,是FeSO4的溶液(A→C稀硫酸过量)与双氧水在酸性溶液中反应,亚铁离子被过氧化氢氧化为三价铁,过氧化氢被还原为水,离子方程式:
2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(4)D为Fe2(SO4)3,溶液中有Fe3+,可取少量D于试管中,用胶头滴管滴入KSCN溶液,出现血红色,说明有Fe3+,
故答案为:取少量D于试管中,用胶头滴管滴入KSCN溶液,出现血红色,说明有Fe3+;
(5)在C(FeSO4)溶液中加入与C等物质的量的Na2O2,恰好使C转化为F(Fe(OH)3),反应的离子方程式为:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+;
故答案为:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+;
(1)红褐色液体是氢氧化铁胶体,分散质粒子直径大小的范围是1nm-100nm,
故答案为:1nm-100nm;
(2)依据推断可知A为Fe,B的化学式为:FeS,H为H2SO4(稀);
故答案为:Fe,FeS,H2SO4(稀);
(3)①因为H2O2是共价化合物,所以分子的电子式为:
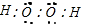 ;
;故答案为:
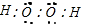 ;
;②C的酸性溶液与双氧水反应,是FeSO4的溶液(A→C稀硫酸过量)与双氧水在酸性溶液中反应,亚铁离子被过氧化氢氧化为三价铁,过氧化氢被还原为水,离子方程式:
2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(4)D为Fe2(SO4)3,溶液中有Fe3+,可取少量D于试管中,用胶头滴管滴入KSCN溶液,出现血红色,说明有Fe3+,
故答案为:取少量D于试管中,用胶头滴管滴入KSCN溶液,出现血红色,说明有Fe3+;
(5)在C(FeSO4)溶液中加入与C等物质的量的Na2O2,恰好使C转化为F(Fe(OH)3),反应的离子方程式为:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+;
故答案为:4Fe2++4Na2O2+6H2O═4Fe(OH)3+O2↑+8Na+;
点评:本题考查了无机物质的推断,物质转化关系的突破推断,主要考查铁及其化合物的性质应用,氧化还原反应的判断和书写离子方程式,关键是浓硫酸和硫化亚铁反应的离子方程式的书写,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在反应 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,被氧化与未被氧化的HCl的质量之比为( )
| A、1:1 | B、8:5 |
| C、5:8 | D、5:3 |
下列各溶液不能与铜发生反应的是( )
| A、浓盐酸 |
| B、浓H2SO4 |
| C、浓硝酸 |
| D、稀硝酸 |
在25℃下,将a mol?L-1的醋酸(HAc)与0.01mol?L-1的氢氧化钠溶液等体积混合,反应平衡时溶液呈中性.则下列说法中,不正确的是( )
| A、此时醋酸和氢氧化钠溶液恰好中和 | ||
| B、溶液中存在未电离的醋酸分子 | ||
C、用含a的代数式表示醋酸(HAc)的电离常数为Ka=
| ||
| D、a肯定大于0.01 |
下列说法错误的是( )
| A、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| B、硅酸盐NaAISiO4.nH2O可改写成氧化物形式为:Na2O.AI2O3.2SiO2.2nH2O |
| C、AI65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属Al、Cu、Fe都大 |
| D、过量铁与浓硫酸加热反应可以得到氢气 |
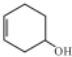 )能发生多种不同反应;回答下列问题:
)能发生多种不同反应;回答下列问题: