题目内容
下列不能说明氯的非金属性比硫强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S ⑤在与钠反应时,S原子得到的电子数更多
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS ⑦HCl酸性比H2S强.
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S ⑤在与钠反应时,S原子得到的电子数更多
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS ⑦HCl酸性比H2S强.
| A、②⑤⑦ | B、①②⑦ |
| C、②⑤⑥ | D、③④⑤ |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:
分析:比较非金属性的强弱,可根据①氢化物的稳定性,②最高价氧化物对应的水化物的酸性,③对应的单质的氧化性,④单质之间的置换反应⑤与氢气反应的剧烈程度等判断.
解答:
解:①元素的非金属性越强,对应的氢化物越稳定,HCl比H2S稳定,可说明非金属性:Cl>S,故①正确;
②HClO氧化性比H2SO4强不能作为比较非金属性强弱的依据,故②错误;
③元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,HClO4酸性比H2SO4强,可说明非金属性:Cl>S,故③正确;
④Cl2能与H2S反应生成S,可说明氧化性:Cl2>S,单质的氧化性越强,对应元素的非金属性越强,故④正确;
⑤不能以最外层电子数的多少判断非金属性的强弱,故⑤错误;
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS,可说明氧化性:Cl2>S,单质的氧化性越强,对应元素的非金属性越强,故⑥正确;
⑦比较非金属性的强弱,应根据对应的最高价氧化物对应的水化物的酸性比较,不能根据氢化物的酸性进行比较,例如HF的酸性比HCl弱,但非金属性F大于Cl,故⑦错误.
故选A.
②HClO氧化性比H2SO4强不能作为比较非金属性强弱的依据,故②错误;
③元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,HClO4酸性比H2SO4强,可说明非金属性:Cl>S,故③正确;
④Cl2能与H2S反应生成S,可说明氧化性:Cl2>S,单质的氧化性越强,对应元素的非金属性越强,故④正确;
⑤不能以最外层电子数的多少判断非金属性的强弱,故⑤错误;
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS,可说明氧化性:Cl2>S,单质的氧化性越强,对应元素的非金属性越强,故⑥正确;
⑦比较非金属性的强弱,应根据对应的最高价氧化物对应的水化物的酸性比较,不能根据氢化物的酸性进行比较,例如HF的酸性比HCl弱,但非金属性F大于Cl,故⑦错误.
故选A.
点评:本题考查非金属性的强弱比较,题目难度不大,注意比较非金属性的角度和方法.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
已知某有机物C6H12O2能发生水解反应生成A和B,B能氧化成A,则B的结构式可能有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下列有关元素的性质及其递变规律正确的是( )
| A、IA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B、第二周期元素从左到右,最高正价从+1递增到+7 |
| C、同主族元素的简单阴离子还原性越强,对应单质的氧化性也越强 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
某微粒用
Rn+表示,下列关于该微粒叙述正确的是( )
A Z |
| A、所含质量数=A-n |
| B、所含中子数=A-Z |
| C、所含电子数=Z+n |
| D、所含质子数=A+Z |
下列化学用语正确的是( )
| A、乙烯的结构简式为:CH2CH2 |
| B、苯酚的分子式为:C6H6O |
| C、羟基的电子式为:-O﹕H |
D、甲烷分子的比例模型: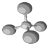 |
下列有关氢化物的叙述中正确的是( )
| A、稳定性:H2S>HF |
B、HCl的电子式为: |
| C、一个D2O分子所含的中子数为8 |
| D、在卤化氢中HF最稳定 |