题目内容
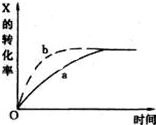 如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A、升高温度 | B、加大X的投入 |
| C、加催化剂 | D、增大体积 |
考点:转化率随温度、压强的变化曲线
专题:
分析:图中给出的是X转化率随着反应时间的变化关系,从图中a、b两条曲线可以看出二者达到平衡时的X的转化率相同,说明改变条件后平衡不发生移动,但是达到平衡用的时间不同,b曲线先达到平衡,说明改变条件后反应速率快;
分析影响化学反应速率的因素和影响化学平衡移动的因素,要想加快反应速率但是平衡不移动,可能的条件是:一使用催化剂;二加压(只对反应前后气体体积不变的反应).
分析影响化学反应速率的因素和影响化学平衡移动的因素,要想加快反应速率但是平衡不移动,可能的条件是:一使用催化剂;二加压(只对反应前后气体体积不变的反应).
解答:
解:A.升高温度,反应速率加快,平衡逆向移动,故A错误;
B.加大X的投入,反应速率加快,平衡正向移动,故B错误;
C.加催化剂,反应速率加快,平衡不移动,故C正确;
D.该反应前后气体体积不变,增大体积,反应速率减慢,平衡不移动,故D错误;
故选C.
B.加大X的投入,反应速率加快,平衡正向移动,故B错误;
C.加催化剂,反应速率加快,平衡不移动,故C正确;
D.该反应前后气体体积不变,增大体积,反应速率减慢,平衡不移动,故D错误;
故选C.
点评:本题结合图象考查影响化学速率和化学平衡移动的因素,难度中等,要注意基础知识的积累.

练习册系列答案
相关题目
现有100mL只含MgCl2和AlCl3两种溶质的混合溶液,其中c(Cl-)=1.0mol?L-1,c(Mg2+)=0.35mol?L-1要使其中的Mg2+全部转化为Mg(OH)2沉淀而分离出来,至少需要2mol?L-1的NaOH溶液的体积是( )
| A、25mL | B、35mL |
| C、45mL | D、55mL |
下列说法不正确的是( )
| A、化石燃料是不可再生的,在地球上的蕴藏量是有限的 |
| B、化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| C、直接燃烧煤不如将煤进行深加工后再燃烧的效果好 |
| D、将煤处理后变成气体燃料的目的是提高煤的价格 |
将pH=2的盐酸和pH=12的氨水等体积混合后,在所得的混合溶液中,下列关系式正确的是( )
| A、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| D、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
已知25℃时,KHF=7.2×10-4 KHCN=4.9×10-10 KHNO2=4.6×10-4 KCH3COOH=1.8×10-5则相同浓度的上述溶液中溶质分子浓度最大的是( )
| A、HF |
| B、HCN |
| C、HNO2 |
| D、CH3COOH |
某温度下,在恒容密闭容器中充入NO2,发生反应2NO2(g)?N2O4(g)△H<0,达到平衡后,下列说法不正确的是( )
| A、再充入少量NO2,达平衡后NO2的转化率升高 |
| B、再充入少量NO2,达平衡后NO2的体积分数增大 |
| C、再充入少量N2O4,达平衡后NO2的体积分数减小 |
| D、升高温度,体系的颜色加深 |
下列说法错误的是( )
| A、二氧化硅是光导纤维的主要原料 |
| B、硅是信息技术的关键材料 |
| C、陶瓷餐具所用材料为硅酸盐 |
| D、水晶镜片所用原料为硅酸盐 |
测知由Fe2(SO4)3和FeSO4组成混合物中含硫a%,则其含铁量应为( )
| A、(100-4a)% |
| B、(100-2a)% |
| C、(100-a)% |
| D、(100-3a)% |