题目内容
现有下列各组溶液:
①10℃时10mL 0.1mol/L的Na2S2O3溶液和?50mL 0.05 mol/L的H2SO4溶液;
②10℃时10mL 0.05mol/L的Na2S2O3溶液和?10mL 0.1mol/L的H2SO4溶液;
③30℃时 10mL 0.05mol/L的Na2S2O3溶液和?10mL 0.1mol/L的H2SO4溶液.
若同时将它们混合发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O则出现浑浊的先后次序是( )
①10℃时10mL 0.1mol/L的Na2S2O3溶液和?50mL 0.05 mol/L的H2SO4溶液;
②10℃时10mL 0.05mol/L的Na2S2O3溶液和?10mL 0.1mol/L的H2SO4溶液;
③30℃时 10mL 0.05mol/L的Na2S2O3溶液和?10mL 0.1mol/L的H2SO4溶液.
若同时将它们混合发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O则出现浑浊的先后次序是( )
| A、①②③ | B、②①③ |
| C、③②① | D、①③② |
考点:化学反应速率的影响因素,含硫物质的性质及综合应用
专题:化学反应速率专题
分析:温度越高、浓度越大,则反应速率就越快,在实验中就最先出现浑浊,以此解答该题.
解答:
解:③反应温度最高,则速率最大,①②相比较,温度相同,②浓度较大,则②反应速率较大,所以反应速率由大到校的顺序为③②①,
故选C.
故选C.
点评:本题考查影响化学反应速率的因素,明确温度和浓度对化学反应速率的影响即可解答,注意利用表格中的数据来比较温度和浓度.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
室温下将等物质的量的NaCN和HCN溶于一定量水中,再加入适量稀盐酸,调整溶液pH=7.下列说法正确的是( )
| A、未加入稀盐酸之前c( CN-)>c(HCN) | ||
B、加稀盐酸后溶液中
| ||
| C、pH=7时,溶液中c( Na+)=c( CN-) | ||
| D、加稀盐酸后HCN的电离程度减小,但c( H+)增大 |
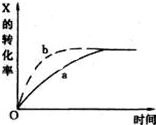 如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A、升高温度 | B、加大X的投入 |
| C、加催化剂 | D、增大体积 |
制造光导纤维的主要原料是( )
| A、晶体硅 | B、二氧化硅 |
| C、石墨 | D、硅酸钠 |
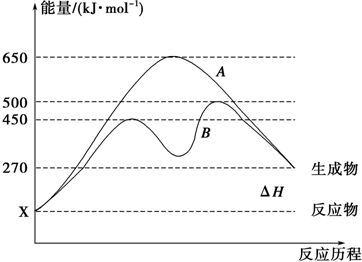
关于热化学方程式:2H2(g)+02(g)=2H20(1),△H=-571.6kJ?mol-1,下列有关叙述不正确的是( )
| A、2mol H2完全燃烧生成液态水时放出571.6 kJ的热 | ||
| B、1mol H2完全燃烧生成液态水时放出285.8kJ的热 | ||
| C、2个氢分子完全燃烧生成液态水时放出571.6 kJ的热 | ||
D、上述热化学方程式可表示为H2(g)+
|