题目内容
不可能通过观察法了解的金属钠的性质是( )
| A、钠是一种银白色金属 |
| B、熔点为97.81℃,密度为0.97 g?cm-3 |
| C、钠与H2O剧烈反应 |
| D、钠在室温下氧化和在空气中燃烧得到不同的产物 |
考点:钠的化学性质,钠的物理性质
专题:
分析:A、金属的颜色可以观察得到;
B、物质的熔点和密度是物质的本质特点,不能用眼看出;
C、反应的剧烈程度可以根据反应现象得出;
D、金属钠在空气中得到的氧化钠是白色的,加热得到的过氧化钠是淡黄色的.
B、物质的熔点和密度是物质的本质特点,不能用眼看出;
C、反应的剧烈程度可以根据反应现象得出;
D、金属钠在空气中得到的氧化钠是白色的,加热得到的过氧化钠是淡黄色的.
解答:
解:A、金属的颜色是银白色的,有金属光泽,可以观察得到,故A错误;
B、物质的熔点和密度是物质的本质特点,不能用眼看出,故B正确;
C、反应的剧烈程度可以根据反应现象得出,属于眼睛可看的内容,故C错误;
D、金属钠在空气中得到的氧化钠是白色的,加热得到的过氧化钠是淡黄色的,颜色不同,可以看出,故D错误.
故选B.
B、物质的熔点和密度是物质的本质特点,不能用眼看出,故B正确;
C、反应的剧烈程度可以根据反应现象得出,属于眼睛可看的内容,故C错误;
D、金属钠在空气中得到的氧化钠是白色的,加热得到的过氧化钠是淡黄色的,颜色不同,可以看出,故D错误.
故选B.
点评:本题考查学生对观察法的理解和应用,注意物质的物理性质中有的可以根据眼睛看出,但是有的不可以,难度不大.

练习册系列答案
相关题目
已知某物质X能发生如图转化:X
Y
Z
A,下列有关上述转化关系中物质及其反应的叙述不正确的是( )
| O2 |
| ① |
| O2 |
| ② |
| H2O |
| ③ |
| A、若X为N2或NH3,则A为硝酸 |
| B、若X为S或H2S,则A为硫酸 |
| C、若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y |
| D、反应①和一定为氧化还原反应,反应一定为非氧化还原反应 |
常温下,若HA溶液和NaOH溶液混合后pH=7,下列说法不合理的是( )
| A、反应后HA溶液可能有剩余 |
| B、生成物NaA的水溶液的pH可能小于7 |
| C、HA溶液和NaOH溶液的体积可能不相等 |
| D、HA溶液的c(H+)和NaOH溶液的c(OH-) 可能不相等 |
下列关于Na2CO3和NaHCO3的性质的比较中,正确的是( )
| A、热稳定性:Na2CO3>NaHCO3 |
| B、常温时在水中的溶解度:NaHCO3>Na2CO3 |
| C、与稀盐酸反应的剧烈程度:Na2CO3>NaHCO3 |
| D、等质量的固体与足量盐酸反应放出CO2的质量:Na2CO3>NaHCO3 |
蓝色的氮化硅硬度大、熔点高、性质稳定,根据性质推测,它不可能的用途是( )
| A、制备光导纤维 |
| B、制汽轮机叶片 |
| C、制永久性模具 |
| D、制造柴油机 |
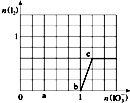 已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示.则下列有关说法正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示.则下列有关说法正确的是( )| A、b点时的还原产物可能是I2 |
| B、当n(KIO3)=1.1mol时,溶液中n(I-)=0.5mol |
| C、a点时剩余NaHSO3的物质的量为1.2mol |
| D、反应过程中的氧化反应所得产物均为SO42- |
