题目内容
15.下列实验操作和现象对应的结论错误的是( )| 选项 | 实验操作和现象 | 结论 |
| A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
| B | 物质的量之比为2:3的稀硝酸和稀硫酸 | 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO |
| C | 向1mL浓度均为0.05mol•L-1NaCl、NaI的混合溶液中滴加2滴0.01mol•L-1 AgNO3溶液,振荡,沉淀是黄色 | Ksp(AgCl)<Ksp(AgI) |
| D | 室温下,用pH试纸测得0.1mol•L-1NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.白色沉淀为AgCl或硫酸钡;
B.Cu过量,硫酸根离子不反应,Cu、硝酸根离子、氢离子以3:2:8反应;
C.混合溶液中滴加2滴0.01mol•L-1 AgNO3溶液,Ksp小的先沉淀;
D.pH约为5,溶液显酸性.
解答 解:A.白色沉淀为AgCl或硫酸钡,则溶液X中可能含有SO42-,故A正确;
B.Cu过量,硫酸根离子不反应,Cu、硝酸根离子、氢离子以3:2:8发生氧化还原反应,则反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO,故B正确;
C.混合溶液中滴加2滴0.01mol•L-1 AgNO3溶液,Ksp小的先沉淀,则Ksp(AgCl)>Ksp(AgI),故C错误;
D.pH约为5,溶液显酸性,可知HSO3-的电离程度大于其水解程度,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握离子检验、沉淀生成、氧化还原反应、电离与水解、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
5.某同学将光亮镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生.为探究该反应原理,该同学做了以下试验并观察到相关现象,由此得出的结论不合理的是( )
| 选项 | 实验及现象 | 结论 |
| A | 将湿润红色石蕊试纸靠近试管口 | 反应中有NH3产生 |
| B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产生 |
| C | 收集气体的同时测得溶液的pH为8.0 | 生成Mg(OH)2使溶液呈弱碱性 |
| D | 向NH4Cl溶液中加锌,也有大量气泡产生 | 活泼金属可促进NH4+水解 |
| A. | A | B. | B | C. | C | D. | D |
3.下列各项中的方程式不能正确解释对应的原因或现象的是( )
| A. | 盛放碱液的试剂瓶不用玻璃塞;SiO2+2OH-═SiO32-+H2O | |
| B. | 配制FeCl3溶液时要加盐酸:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 制Cl2时用排饱和氯化钠溶液收集气体:H2O+Cl2?Cl-+H++HClO | |
| D. | 金属钠燃烧时,火焰呈黄色:2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$Na2O2 |
10.下列说法中正确的是( )
| A. | 将苯加入溴水中振荡后,水层接近无色,是因为发生了取代反应 | |
| B. | 一体积某气态烃与HC1充分加成消耗HC1一体积,加成后的物质最多还能和5体积氯气发生取代反应,由此推断原气态烃是乙烯 | |
| C. | 环己醇能与氢氧化钠溶液反应且所有碳原子可以共面 | |
| D. | 等质量的乙烯和乙醇在氧气中充分燃烧后耗氧量相同. |
20.对下列实验现象解释正确的是( )
| 实验内容 | 实验现象 | 相关解释 | |
| A | 等量的Cu分别与等体积足量的浓硝酸和稀硝酸反应 | 浓硝酸反应后呈绿色,稀硝酸反应后呈蓝色 | c(Cu2+)不同 |
| B | NH3与Cl2混合 | 生成白烟 | NH3与Cl2发生化合反应生成NH4Cl |
| C | 往Fe(OH)3胶体中逐滴滴入稀盐酸 | 先出现红褐色沉淀,后沉淀溶解 | 先胶体聚沉,后Fe(OH)3溶解 |
| D | 加热硝酸铜固体,将带火星的木条伸入所得的气体中 | 生成红棕色气体,带火星木条复燃 | 2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑有氧气生成,不能说明NO2有助燃性. |
| A. | A | B. | B | C. | C | D. | D |
4.下列说法正确的是( )
| A. | pH=6的溶液一定显酸性 | |
| B. | 25℃时,0.1mol/L的NaHB溶液呈酸性,说明H2B为强酸 | |
| C. | NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | |
| D. | 0.1mol/L CH3COOH和0.05mol/L NaOH溶液等体积混合,所得溶液中:2c(Na+)═c(CH3COO-)+c(CH3COOH) |
18.下列说法中正确的是( )
| A. | pH=2的盐酸溶液稀释100倍,pH=0 | |
| B. | pH=12的氢氧化钠溶液稀释10倍,pH=13 | |
| C. | pH=5的硫酸溶液稀释1000倍,pH=8 | |
| D. | pH=3的盐酸溶液稀释10倍,pH=4 |
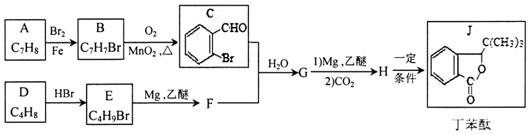
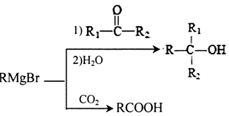
 .H发生缩聚反应生成的高分子化合物的结构简式为
.H发生缩聚反应生成的高分子化合物的结构简式为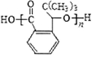 .
.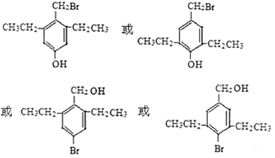 .
.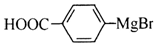 能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.
能与CO2反应生成有机物M.符合下列条件的M的同分异构体共有10种.