题目内容
10.下列说法中正确的是( )| A. | 将苯加入溴水中振荡后,水层接近无色,是因为发生了取代反应 | |
| B. | 一体积某气态烃与HC1充分加成消耗HC1一体积,加成后的物质最多还能和5体积氯气发生取代反应,由此推断原气态烃是乙烯 | |
| C. | 环己醇能与氢氧化钠溶液反应且所有碳原子可以共面 | |
| D. | 等质量的乙烯和乙醇在氧气中充分燃烧后耗氧量相同. |
分析 A.苯与溴水不反应;
B.一体积某气态烃与HC1充分加成消耗HC1一体积,说明含有碳碳双键,加成后的物质最多还能和5体积氯气发生取代反应,说明加成产物含有5个H原子;
C.环己醇与氢氧化钠溶液不反应;
D.等物质的量时,耗氧量相同.
解答 解:A.苯与溴水不反应,溴易溶于苯,为萃取现象,但没有发生化学反应,故A错误;
B.一体积某气态烃与HC1充分加成消耗HC1一体积,说明含有碳碳双键,加成后的物质最多还能和5体积氯气发生取代反应,说明加成产物含有5个H原子,则原烃含有4个H,为乙烯,故B正确;
C.环己醇与氢氧化钠溶液不反应,故C错误;
D.乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可拆写成C2H4•H2O,“CxHy”相同,等物质的量时耗氧量相等,但二者相对分子质量不等,则等质量时耗氧量不同,故D错误.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的组成、结构特点以及官能团的性质,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.常温下能用铁罐或铝罐贮存的是( )
| A. | 浓H2SO4 | B. | 浓HCl | C. | 稀H2SO4 | D. | 稀HNO3 |
18.工业上常用亚硝酸钠(NaNO2)作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂.某兴趣小组用下列装置制备NaNO2并探究NO、NO2的某一化学性质(A中加热装置已略去).
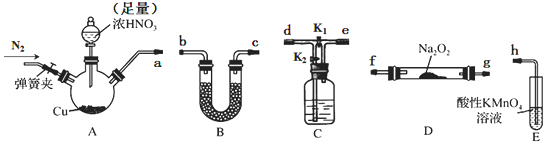
已知:
①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+.
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+4NO2↑+2H2O.
(2)用图中的装置制备NaNO2,其连接顺序为:a→debcfg(b与c、f与g可以交换→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作关闭K1,打开K2.
(3)E装置发生反应的离子方程式是3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O.
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应.某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究.
步骤②操作的目的是排尽装置中残留的NO2;步骤③C瓶中发生的化学方程式为3NO2+H2O=2HNO3+NO;
通过实验可以得出:NO(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色.

已知:
①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+.
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+4NO2↑+2H2O.
(2)用图中的装置制备NaNO2,其连接顺序为:a→debcfg(b与c、f与g可以交换→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作关闭K1,打开K2.
(3)E装置发生反应的离子方程式是3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O.
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应.某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究.
| 步骤 | 操作及现象 |
| ① | 关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色. |
| ② | 停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间. |
| ③ | 更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同. |
通过实验可以得出:NO(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色.
5.下列选项中的操作、现象与结论完全一致的是( )
| 操作 | 现象 | 结论 | |
| A | 向滴有酚酞的NaOH溶液中通入 Cl2 | 溶液褪色 | HClO有漂白性 |
| B | 无水乙醇与浓硫酸共热至170℃,将产生气体通入溴水 | 溴水褪色 | 乙烯和溴水发生加成反应 |
| C | 向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色深 | 结合H+能力: CO32->HCO3- |
| D | 用发光小灯泡分别做HCl和CH3COOH导电性实验 | 发光强度:HCl强于CH3COOH | CH3COOH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
15.下列实验操作和现象对应的结论错误的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
| B | 物质的量之比为2:3的稀硝酸和稀硫酸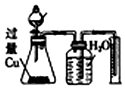 | 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO |
| C | 向1mL浓度均为0.05mol•L-1NaCl、NaI的混合溶液中滴加2滴0.01mol•L-1 AgNO3溶液,振荡,沉淀是黄色 | Ksp(AgCl)<Ksp(AgI) |
| D | 室温下,用pH试纸测得0.1mol•L-1NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
| A. | A | B. | B | C. | C | D. | D |
2.下列关于有机化合物的说法正确的是( )
| A. | 右图为某烃的球棍模型,其分子中C-C键的数目为8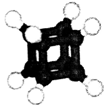 | |
| B. | 由乙烯制取氯乙烷属于取代反应 | |
| C. | C7H7C1属于芳香族化合物的同分异构体有4种 | |
| D. | 丙烯腈(CH2=CH-CN)通过加聚反应制得人造羊毛,其成分与天然羊毛相同 |
19.已知松油醇的结构简式如图,下列说法错误的是( )
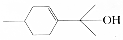

| A. | 松油醇的分子式为C10H18O | B. | 松油醇分子只含一种官能团 | ||
| C. | 松油醇能使酸性KMnO4溶液褪色 | D. | 松油醇能发生取代反应和加成反应 |
13.某温度下,0.01mol/L NaOH的pH为10,该温度下将pH=5的强酸溶液和pH=8的强碱溶液混合后pH=7,则酸溶液体积和碱溶液体积比为( )
| A. | 1:10 | B. | 10:1 | C. | 9:2 | D. | 2:9 |
 CH3COOC2H5+H2O (条件:浓硫酸做催化剂,加热)
CH3COOC2H5+H2O (条件:浓硫酸做催化剂,加热)