题目内容
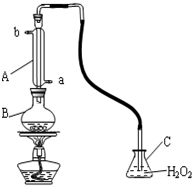 中华人民共和国国家标准规定葡萄酒中SO2最大使用量为0.25g?L-1.某兴趣小组用右图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.(可能用到的相对原子质量:H-1 O-16 S-32)
中华人民共和国国家标准规定葡萄酒中SO2最大使用量为0.25g?L-1.某兴趣小组用右图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.(可能用到的相对原子质量:H-1 O-16 S-32)(1)仪器B的名称是
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,写出该反应的离子方程式:
(3)除去C中过量的H2O2,然后用0.0900mol?L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为
①检查滴定管是否漏水
②用标准液润洗盛标准液的滴定管
③装标准溶液并调整液面(记录初读数)
④用蒸馏水洗涤玻璃仪器
⑤把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇至滴定终点,记下滴定管液面刻度.
则滴定操作的正确顺序是(用序号填写)
(4)用标准NaOH溶液滴定时,以下操作引起误差偏大的是
A.滴定前仰视,滴定后俯视
B.盛标准液的滴定管用蒸馏水洗后未用标准液润洗
C.颜色改变立即读数
D.盛标准液的滴定管滴前尖嘴部分有气泡,终了无气泡
(5)滴定至终点时,消耗NaOH溶液20.00mL,该葡萄酒中SO2含量为
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)根据仪器B的形状和用途分析为圆底烧瓶,仪器A特点和用途分析,为了充分冷却气体,应该逆流;
(2)二氧化硫具有还原性,能够与实验室反应生成硫酸,据此写出反应的离子方程式;
(3)根据滴定终点时溶液的pH及常见指示剂的变色范围选用正确的指示剂;根据滴定过程分析,滴定准备阶段,滴定实验过程阶段检漏、润洗、装液、充液、调液、读数,滴定至终点读取数值,计算得到;
(4)滴定误差分析的依据是,c(待测)=
,标准溶液体积增大,测定结果偏高,据此分析选项;
(5)根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;
(2)二氧化硫具有还原性,能够与实验室反应生成硫酸,据此写出反应的离子方程式;
(3)根据滴定终点时溶液的pH及常见指示剂的变色范围选用正确的指示剂;根据滴定过程分析,滴定准备阶段,滴定实验过程阶段检漏、润洗、装液、充液、调液、读数,滴定至终点读取数值,计算得到;
(4)滴定误差分析的依据是,c(待测)=
| c(标准)V(标准) |
| V(待测) |
(5)根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;
解答:
解:(1)根据仪器的构造可知,仪器B为烧瓶或圆底烧瓶,仪器A为冷凝管,冷凝管中通水方向采用逆向通水法,冷凝效果最佳,所以应该进水口为a,
故答案为:烧瓶或圆底烧瓶;a;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的离子方程式为:SO2+H2O2=2H++SO42-,
故答案为:SO2+H2O2=2H++SO42-;
(3)滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0),根据滴定过程分析,滴定准备阶段,滴定实验过程阶段检漏、润洗、装液、充液、调液、读数,滴定至终点读取数值,计算得到,滴定操作的正确顺序是①检查滴定管是否漏水,④用蒸馏水洗涤玻璃仪器,②用标准液润洗盛标准液的滴定管,③装标准溶液并调整液面(记录初读数),⑤把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇至滴定终点,记下滴定管液面刻度;
故答案为:酚酞; ①④②③⑤;
(3)滴定误差分析的依据是,c(待测)=
,
A.滴定前仰视,滴定后俯视 读取标准溶液体积减小,测定结果减小,故A不符合;
B.盛标准液的滴定管用蒸馏水洗后未用标准液润洗,消耗标准溶液体积增大,测定结构偏高,故B正确;
C.颜色改变立即读数,可能未达到反应终点,标准溶液体积减小,测定结果偏低,故C不符合;
D.盛标准液的滴定管滴前尖嘴部分有气泡,终了无气泡,标准溶液消耗体积增大,测定结果偏高,故D正确;
故选BD.
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:,
×0.0900mol/L×0.020L×64g/mol=0.0576g,该葡萄酒中的二氧化硫含量为:
=0.192g/L,
故答案为:0.192;
故答案为:烧瓶或圆底烧瓶;a;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的离子方程式为:SO2+H2O2=2H++SO42-,
故答案为:SO2+H2O2=2H++SO42-;
(3)滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0),根据滴定过程分析,滴定准备阶段,滴定实验过程阶段检漏、润洗、装液、充液、调液、读数,滴定至终点读取数值,计算得到,滴定操作的正确顺序是①检查滴定管是否漏水,④用蒸馏水洗涤玻璃仪器,②用标准液润洗盛标准液的滴定管,③装标准溶液并调整液面(记录初读数),⑤把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇至滴定终点,记下滴定管液面刻度;
故答案为:酚酞; ①④②③⑤;
(3)滴定误差分析的依据是,c(待测)=
| c(标准)V(标准) |
| V(待测) |
A.滴定前仰视,滴定后俯视 读取标准溶液体积减小,测定结果减小,故A不符合;
B.盛标准液的滴定管用蒸馏水洗后未用标准液润洗,消耗标准溶液体积增大,测定结构偏高,故B正确;
C.颜色改变立即读数,可能未达到反应终点,标准溶液体积减小,测定结果偏低,故C不符合;
D.盛标准液的滴定管滴前尖嘴部分有气泡,终了无气泡,标准溶液消耗体积增大,测定结果偏高,故D正确;
故选BD.
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:,
| 1 |
| 2 |
| 0.0576g |
| 0.3L |
故答案为:0.192;
点评:本题考查了探究物质的组成、测量物质的含量的方法,题目难度中等,试题涉及了二氧化硫性质、中和滴定的计算,要求学生掌握探究物质组成、测量物质含量的方法,明确二氧化硫的化学性质及中和滴定的操作方法及计算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列说法中不正确的是( )
| A、普通玻璃呈淡绿色是由于含Fe2+ |
| B、坩埚、蒸发皿都属于陶瓷制品 |
| C、唐“三彩”是一种玻璃制品 |
| D、高温下硅酸钙比碳酸钙稳定 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、100mL 1mol/L FeCl3溶液中含阳离子数为0.1NA |
| B、常温常压下1 mol NO2气体与水反应生成NA个NO3-离子 |
| C、0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3NA |
| D、80mL 10mol/L浓盐酸与足量MnO2反应,转移电子数为0.4NA |
依据下列实验,不能证明一元酸HR是弱酸的是( )
| A、室温下NaR溶液的pH大于7 |
| B、加热NaR溶液时,溶液的pH变小 |
| C、稀盐酸中加入少量NaR固体,溶解后溶液的pH变大 |
| D、HR溶液中加少量NaR固体,溶解后溶液的pH变大 |