题目内容
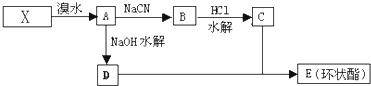
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图1所示:
(1)写出B的结构简式 ;
(2)写出下列反应的化学方程式:反应①: ;反应④:
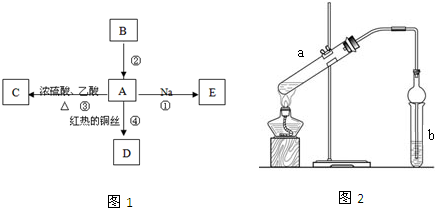
(3)实验室利用反应③制取C,常用图2装置:
(I)a试管中的主要化学反应的方程式: ;反应类型是 .
(Ⅱ)在实验中球形干燥管除起冷凝作用外,另一个重要作用是 .
(Ⅲ)分离试管b中所得产品的操作为(只填名称) .
(1)写出B的结构简式
(2)写出下列反应的化学方程式:反应①:
(3)实验室利用反应③制取C,常用图2装置:
(I)a试管中的主要化学反应的方程式:
(Ⅱ)在实验中球形干燥管除起冷凝作用外,另一个重要作用是
(Ⅲ)分离试管b中所得产品的操作为(只填名称)

考点:有机物的推断,乙酸乙酯的制取
专题:有机物的化学性质及推断
分析:B的产量可衡量一个国家石油化工发展的水平,B是乙烯,A是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,A能与Na、乙酸反应,在红热铜丝发生催化氧化,可推知A是CH3CH2OH,根据框图中的转化关系、反应条件和反应试剂可推得,C是CH3COOCH2CH3,D是2CH3CHO,E是CH3CH2ONa,据此解答.
解答:
解:B的产量可衡量一个国家石油化工发展的水平,B是乙烯,A是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,A能与Na、乙酸反应,在红热铜丝发生催化氧化,可推知A是CH3CH2OH,根据框图中的转化关系、反应条件和反应试剂可推得,C是CH3COOCH2CH3,D是2CH3CHO,E是CH3CH2ONa,
(1)B是乙烯,结构简式为CH2=CH2,
故答案为:CH2=CH2;
(2)反应①是乙醇与钠反应生成乙醇钠与氢气,反应方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
反应④是乙醇在铜作催化剂、加热条件下催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,2CH3CH2OH+O2
2CH3CHO+2H2O;
(3)(Ⅰ)a试管中的主要化学反应是乙酸与乙醇反应生成乙酸乙酯,化学方程式为CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,属于取代反应,
故答案为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O;取代反应;
(Ⅱ)在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止液体倒吸,
故答案为:防止液体倒吸;
(Ⅲ)试管b中收集的是乙酸乙酯,与水不互溶,所以可以用分液方法得到乙酸乙酯,
故答案为:分液.
(1)B是乙烯,结构简式为CH2=CH2,
故答案为:CH2=CH2;
(2)反应①是乙醇与钠反应生成乙醇钠与氢气,反应方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
反应④是乙醇在铜作催化剂、加热条件下催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,2CH3CH2OH+O2
| Cu |
| △ |
(3)(Ⅰ)a试管中的主要化学反应是乙酸与乙醇反应生成乙酸乙酯,化学方程式为CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
故答案为:CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
(Ⅱ)在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止液体倒吸,
故答案为:防止液体倒吸;
(Ⅲ)试管b中收集的是乙酸乙酯,与水不互溶,所以可以用分液方法得到乙酸乙酯,
故答案为:分液.
点评:考查有机推断、乙酸乙酯的制取,涉及烯、醇、羧酸的性质与转化等,难度不大,是对常见有机物知识的简单运用,注意掌握各类有机物的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在任何温度下,纯水都是中性,这是因为纯水中( )
| A、pH=7 |
| B、c(H+)=c(OH-) |
| C、c(H+)=c(OH-)=10-7mol?L-1 |
| D、c(H+)?c(OH-)=1×10-14 |
离子方程式错误的是( )
| A、Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | ||||
| B、向10mL 1.5mol?L-1NaHSO4溶液中加入10mL 1mol?L-1Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O | ||||
| C、工业用石灰乳制漂白粉:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O | ||||
D、向20mL沸水中滴入1mL饱和FeCl3溶液,继续煮沸至溶液呈红褐色:Fe3++3H2O
|
下列离子方程式中正确的是( )
| A、氢氧化钠溶液吸收过量的二氧化碳 OH-+CO2=HCO3- |
| B、亚硫酸氢铵溶液与足量氢氧化钠溶液反应 HSO3-+OH-=SO32-+H2O |
| C、氯气通入冷水中 Cl2+H2O=Cl-+ClO-+2H+ |
| D、碳酸镁悬浊液中加醋酸 CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
下列说法正确的是( )
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | ||||||||||
| B、向Cr2O72-+H2O?2CrO42-+2H+的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色 | ||||||||||
C、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)
| ||||||||||
D、已知:
 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 |
将CH3COOCH=CH2与CH2=C(CH3)COOCH3加聚,再经过适当的反应即可制得强吸水性的高分子X,X吸水后的质量可达其自身质量的数百倍.高分子X已被广泛用于卫生用品和农业上作吸水剂.关于X的下列说法中正确的是( )
| A、X分子中含C=C |
| B、制取X的过程中无小分子生成 |
| C、熔化的X与钠可反应产生H2 |
| D、上述适当的反应类型为加聚反应 |
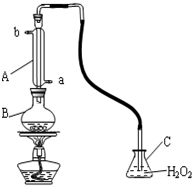 中华人民共和国国家标准规定葡萄酒中SO2最大使用量为0.25g?L-1.某兴趣小组用右图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.(可能用到的相对原子质量:H-1 O-16 S-32)
中华人民共和国国家标准规定葡萄酒中SO2最大使用量为0.25g?L-1.某兴趣小组用右图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.(可能用到的相对原子质量:H-1 O-16 S-32)