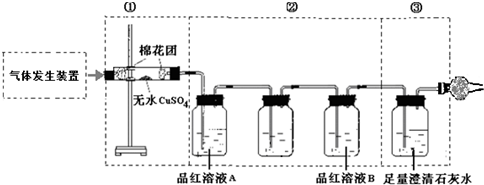
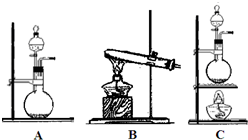
题目内容
17.某电化学气敏传感器工作原理如图所示,下列说法正确的是( )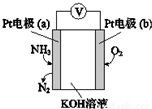
| A. | 该传感器在工作过程中KOH的物质的量不变 | |
| B. | a极的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | b极为负极 |
分析 该感器在工作过程中,负极上氨气失电子生成氮气,则a为负极,氧气在正极上得电子生成氢氧根离子,其电池的总反应为4NH3+3O2═4N2+6H2O,据此分析.
解答 解:A.该传感器在工作过程中总反应为4NH3+3O2═4N2+6H2O,所以KOH的物质的量不变,故A正确;
B.碱性条件下,氨气失电子生成氮气和水,则a极的电极反应式为2NH3+6OH--6e-═N2+6H2O,故B错误;
C.电池的总反应为4NH3+3O2═4N2+6H2O,则反应消耗的NH3与O2的物质的量之比为4:3,故C错误;
D.该感器在工作过程中,负极上氨气失电子生成氮气,则a为负极,故D错误;
故选A.
点评 本题考查了原电池原理,明确正负极上发生的电极反应即可解答,难点是电极反应式的书写,难度中等,侧重于考查学生的分析能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列一组粒子的中心原子杂化类型相同,分子或离子的键角不相等的是( )
| A. | CCl4、SiCl4、SiH4 | B. | H2S、NF3、CH4 | C. | BCl3、NH3、CO2 | D. | SO3、BF3、H3O+ |
5.下列过程一定吸热能量的是( )
| A. | 甲烷的燃烧 | B. | 原子结合成分子 | ||
| C. | 分解反应 | D. | 灼热的碳与二氧化碳反应 |
9.某班学生分组进行了粗盐提纯实验,并对实验结果进行了纯度计算,老师对四组同学计算的产率进行了评价.下列各组同学对造成产率偏高或偏低的原因进行分析,其中正确的是( )
| 产率 | 75% | 65% | 88% | 72% |
| 教师对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 |
| A. | 第1组:过滤时滤纸有气泡 | |
| B. | 第2组:没有蒸发干,精盐中仍然有水分 | |
| C. | 第3组:过滤时滤液高于滤纸的边缘 | |
| D. | 第4组:滤液中还有少量泥沙就开始蒸发 |
6.不能鉴别二氧化碳与二氧化硫的试剂是( )
| A. | 品红溶液 | B. | 酸性高锰酸钾溶液 | ||
| C. | 溴水 | D. | 澄清的石灰水 |
 .
. 互为同分异构体且属于芳香烃的有机物的结构简式
互为同分异构体且属于芳香烃的有机物的结构简式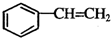 .
. 、
、 .
.