题目内容
14.现有a、b、c、d四种短周期主族元素其原子序数依次增大,a与b位于不同周期,b与c位于相邻主族,c与d同主族.c的原子半径是同周期元素原子中最小的,下列说法不正确的是( )| A. | 简单离子的半径:b>c | B. | 化合物ac是弱电解质 | ||
| C. | 化合物db2可作漂白剂 | D. | 化合物ad的水溶液能蚀刻玻璃. |
分析 a、b、c、d四种短周期主族元素其原子序数依次增大,a与b位于不同周期,b与c位于相邻主族,c与d同主族,则a位于第一周期、b、c位于第二周期、d位于第三周期,故a为H元素;c的原子半径是同周期元素原子中最小的,则c为F元素,c与d同主族,则d为Cl元素;b与c位于相邻主族,b的原子序数小于c,则b为O元素,据此进行解答.
解答 解:a、b、c、d四种短周期主族元素其原子序数依次增大,a与b位于不同周期,b与c位于相邻主族,c与d同主族,则a位于第一周期、b、c位于第二周期、d位于第三周期,故a为H元素;c的原子半径是同周期元素原子中最小的,则c为F元素,c与d同主族,则d为Cl元素;b与c位于相邻主族,b的原子序数小于c,则b为O元素,
A.b、c离子具有相同电子层,离子的核电荷数越大,对应离子半径越小,则离子半径b>c,故A正确;
B.ac为HF,HF在溶液中只能部分电离出氢离子,为弱电解质,故B正确;
C.化合物db2为ClO2,ClO2具有强氧化性,可作漂白剂,故C正确;
D.化合物ad为HCl,HCl的水溶液为盐酸,盐酸不能腐蚀玻璃,故D错误;
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度不大,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
4.向制作印刷电路板的废液中,分别加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 加入过量氨水:NH4+、Cl-、[Cu(NH3)4]2+ | |
| B. | 通入过量Cl2:Fe2+、Cu2+、C-、H+ | |
| C. | 加入过量铁粉:Cu2+、Fe2+、Cl-、H+ | |
| D. | 加入过量KSCN溶液:Na+、K+、Fe3+、H+ |
6.下列实验所用试剂、现象和结论均正确的是( )
| 序号 | 相关实验 | 试剂 | 现象和结论 |
| ① | 鉴别K2CO3和Na2SO4 | 盐酸、澄清的石灰水 | 产生无色无味气体,能使澄清的石灰水变浑浊的是K2CO3 |
| ② | 鉴别NO2和Br2蒸气 | 湿润的淀粉KI试纸 | 试纸变蓝色的是Br2蒸气 |
| ③ | 鉴别葡萄糖和蔗糖 | 银氨溶液 | 有银镜产生的葡萄糖 |
| ④ | 将装满氯水的圆底烧瓶倒置在有氯水的水槽中,日光照射 | -- | 烧瓶内有气泡产生,说明日光照射导致溶解的Cl2逸出 |
| A. | ①③ | B. | ①② | C. | ②④ | D. | ②③ |
9.X、Y、Z、R、W 是原子序数依次增大的五种短周期元素.Y 和 R 同主族,可组成共价化合物 RY2,Y 和 Z 最外层电子数之和与 W 的最外层电子数相同,25℃时,0.1mol/L X 和 W 形成化合物的水溶液 pH=1.下列说法正确的是( )
| A. | 简单离子的半径:Z>R>W>Y | |
| B. | Y、Z、W 三种元素组成的化合物的水溶液可能显碱性 | |
| C. | Z 与 Y、Z 与 W 形成的化合物的化学键完全相同 | |
| D. | WY2、Y3 等可作为新的自来水消毒剂替代 W2,主要原因是 WY2、Y3 的氧化性比 W2 更强 |
19.设NA为阿伏加徳罗常数的值,下列说法不正确的是( )
| A. | 9.2gNO2和N2O4的混合物中含氮原子数目为0.2NA | |
| B. | 常温常压下,35.5g Cl2与足量的NaOH溶液完全反应,转移的电子数为0.5NA | |
| C. | 标准状况下,2.24LNH3与1.6gCH4分子中所含电子数目均为NA | |
| D. | 已知反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ |
1.短周期元素X、Y、Z、M的原子序数依次增大,原子X的L层电子数是K层的2倍,Y2+电子层结构与氖相同,Z原子的质子数为偶数,室温下M单质为淡黄色固体,下列有关说法正确的是( )
| A. | X、Y、Z、M的原子半径依次减小 | |
| B. | Y与M组成化合物的熔点高于X与M组成的化合物 | |
| C. | X、Z、M的最低价气态氢化物的热稳定性依次增强 | |
| D. | X的单质与Y、Z的最高价氧化物均能发生置换反应 |

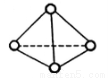 ),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN
),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。